Vlastnosti etheru, struktura, získávání, použití
ethylether, také známý jako diethylether, je organická sloučenina, jejíž chemický vzorec je C4H10O. Vyznačuje se tím, že je bezbarvá a těkavá kapalina, a proto musí být její lahve udržovány co nejhermeticky uzavřené..
Tento ether je klasifikován jako člen dialkyletherů; to znamená, že mají vzorec ROR ', kde R a R' představují různé uhlíkové segmenty. A jak popisuje své střední jméno, diethylether, jsou dva radikály-ethyl ty, které se váží na atom kyslíku.

Zpočátku byl ethyl ether používán jako obecné anestetikum, zavedený v roce 1846 William Thomas Green Morton. Nicméně, kvůli jeho hořlavosti, jeho použití bylo odmítnuto, nahrazovat to jinými méně nebezpečnými anestetiky..
Tato sloučenina byla také použita k odhadu doby krevního oběhu, při hodnocení kardiovaskulárního stavu pacientů.
V těle může být diethylether přeměněn na oxid uhličitý a metabolity; posledně uvedená se vylučuje močí. Většina podaného etheru je však vydechována v plicích, aniž by byla podrobena jakékoli modifikaci.
Na druhé straně se používá jako rozpouštědlo pro mýdla, oleje, parfémy, alkaloidy a gumy.
Index
- 1 Struktura ethyletheru
- 1.1 Mezimolekulární síly
- 2 Fyzikální a chemické vlastnosti
- 2.1 Ostatní názvy
- 2.2 Molekulární vzorec
- 2.3 Molekulová hmotnost
- 2.4 Fyzický vzhled
- 2.5 Vůně
- 2.6 Chuť
- 2.7 Bod varu
- 2.8 Bod tání
- 2.9 Bod vzplanutí
- 2.10 Rozpustnost ve vodě
- 2.11 Rozpustnost v jiných kapalinách
- 2.12 Hustota
- 2.13 Hustota par
- 2.14 Tlak par
- 2.15 Stabilita
- 2.16 Automatické zapalování
- 2.17 Rozklad
- 2.18 Viskozita
- 2.19 Teplo spalování
- 2.20 Teplo odpařování
- 2.21 Povrchové napětí
- 2.22 Ionizační potenciál
- 2.23 Prahová hodnota zápachu
- 2.24 Index lomu
- 3 Získání
- 3.1 Z ethylalkoholu
- 3.2 Z ethylenu
- 4 Toxicita
- 5 Použití
- 5.1 Organické rozpouštědlo
- 5.2 Celková anestézie
- 5.3 Duch etheru
- 5.4 Hodnocení krevního oběhu
- 5.5 Výukové laboratoře
- 6 Odkazy
Struktura ethyletheru
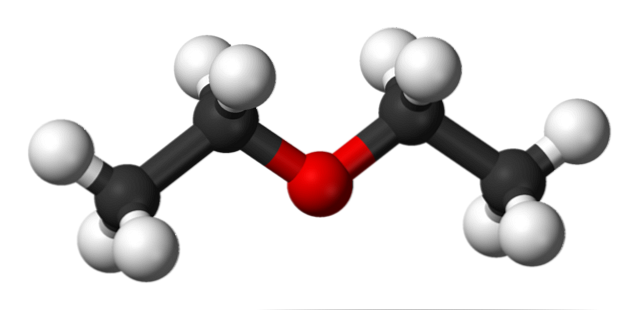
Na obrázku nahoře máme reprezentaci s modelem koulí a tyčí molekulární struktury ethyletheru.
Jak je vidět, červená koule, odpovídající atomu kyslíku, má na obou stranách dvě ethylové skupiny. Všechny spoje jsou jednoduché, ohebné a volně otočné kolem os σ.
Tyto rotace vytvářejí stereoisomery známé jako konformery; že více než izomery jsou alternativními prostorovými stavy. Struktura obrazu přesně odpovídá antikonformátoru, ve kterém jsou všechny jeho skupiny atomů rozloženy (odděleny od sebe).
Jaký by byl další konformer? Zatmění, a přestože váš obraz není k dispozici, vizualizujte ho pouze ve tvaru písmene U. Na horních koncích U by byly umístěny methylové skupiny, -CH3, které by zažily sterické odpudy (kolidovaly by ve vesmíru).
Proto se očekává, že molekula CH3CH2OCH2CH3 přijmout proti konformaci většinu času.
Mezimolekulární síly
Jakými intermolekulárními silami jsou molekuly ethyletheru řízeny v kapalné fázi? Jsou udržovány v kapalině hlavně díky disperzním silám, protože jejich dipólový moment (1,5D) postrádá oblast dostatečně deficientní v elektronické hustotě (δ +)
To proto, že žádný atom uhlíku v ethylových skupinách neposkytuje příliš mnoho elektronové hustoty atomu kyslíku. Výše uvedené je zřejmé z mapy elektrostatického potenciálu ethyl etheru po ruce (spodní obrázek). Všimněte si nepřítomnosti modré oblasti.
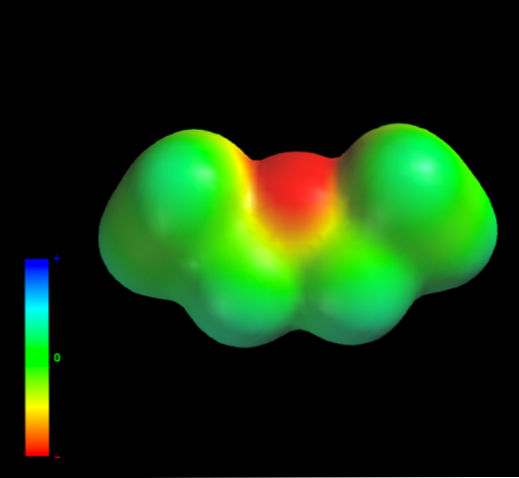
Kyslík nemůže opět tvořit vodíkové vazby, protože v molekulární struktuře nejsou k dispozici žádné vazby O-H. Proto se jedná o okamžité dipóly a jejich molekulovou hmotnost, které upřednostňují jejich disperzní síly.
Navzdory tomu je vysoce rozpustný ve vodě. Proč? Protože jeho atom kyslíku, s vyšší hustotou elektronů, může přijmout vodíkové vazby z molekuly vody:
(CH3CH2)2Oδ- - δ+H-OH
Tyto interakce jsou zodpovědné za 6,04 g tohoto etheru rozpuštěného ve 100 ml vody.
Fyzikální a chemické vlastnosti
Další jména
-Diethylether
-Ethoxyethan
-Ethyl oxid
Molekulární vzorec
C4H100 nebo C2H5)2O.
Molekulová hmotnost
74,14 g / mol.
Fyzický vzhled
Bezbarvá kapalina.
Vůně
Sladká a kořeněná.
Chuť
Hořící a sladké.
Bod varu
94,3 ° F (34,6 ° C) až 760 mmHg.
Teplota tání
-177,3 ° F (-116,3 ° C). Stabilní krystaly.
Bod zapálení
-49 ° F (uzavřený kontejner).
Rozpustnost ve vodě
6,04 g / 100 ml při 25 ° C.
Rozpustnost v jiných kapalinách
Mísitelný s alifatickými alkoholy s krátkým řetězcem, benzenem, chloroformem, petroletherem, rozpouštědlem tuku, mnoha oleji a koncentrovanou kyselinou chlorovodíkovou.
Rozpustný v acetonu a velmi rozpustný v ethanolu. Je také rozpustný v nafta, benzenu a olejích.
Hustota
0,714 mg / ml při teplotě 68 ° F (20 ° C).
Hustota par
2,55 (ve vztahu k vzduchu odebranému s hustotou 1).
Tlak páry
442 mmHg při 68 ° F. 538 mmHg při 25 ° C. 58,6 kPa při 20 ° C.
Stabilita
Pomalu se oxiduje působením vzduchu, vlhkosti a světla s tvorbou peroxidů.
K tvorbě peroxidů může docházet v etherových nádobách, které byly otevřeny a které zůstávají skladovány déle než šest měsíců. Peroxidy mohou vybuchnout třením, nárazem nebo zahřátím.
Zabraňte kontaktu s: zinek, halogeny, nekovovými oxyhalogenidy, silnými oxidačními činidly, chromylchloridem, tementinovými oleji, nitráty a chloridy kovů.
Automatické zapalování
180 ° C (180 ° C).
Rozklad
Při zahřívání se rozkládá, vydává pronikavý a dráždivý kouř.
Viskozita
0,2448 cPoise při 20 ° C.
Teplo spalování
8,807 Kcal / g.
Odpařovací teplo
89,8 cal / g při 30 ° C.
Povrchové napětí
17,06 dyn / cm při 20 ° C.
Ionizační potenciál
9,53 eV.
Prahová hodnota zápachu
0,83 ppm (čistota není uvedena).
Index lomu
1,355 při 15 ° C.
Získání
Z ethylalkoholu
Ethylether lze získat z ethylalkoholu v přítomnosti kyseliny sírové jako katalyzátoru. Kyselina sírová ve vodném prostředí disociuje produkci hydroniového iontu, H3O+.
Bezvodý ethylalkohol protéká roztokem kyseliny sírové, zahřívá se mezi 130 ° C a 140 ° C za vzniku protonace molekul ethylalkoholu. Následně další molekula neprotonovaného ethylalkoholu reaguje s protonovanou molekulou.
Když se to stane, nukleofilní atak druhé molekuly ethylalkoholu podporuje uvolňování vody z první molekuly (protonované); v důsledku toho se vytvoří protonovaný ethylether (CH3CH2OHCH2CH3), s částečně nabitým pozitivním kyslíkem.
Tento způsob syntézy však ztrácí účinnost, protože kyselina sírová se ředí vodou produkovanou v procesu (produkt dehydratace ethylalkoholu)..
Teplota reakce je kritická. Při teplotách pod 130 ° C je reakce pomalá a ethylalkohol bude destilován.
Při teplotě vyšší než 150 ° C způsobuje kyselina sírová tvorbu ethylenu (alkénu s dvojnou vazbou) namísto kombinace s ethylalkoholem za vzniku ethyletheru..
Z ethylenu
V opačném procesu, to znamená hydrataci ethylenu v plynné fázi, může být vedle ethylalkoholu vytvořen jako vedlejší produkt ethylether. Ve skutečnosti tato syntetická cesta produkuje většinu této organické sloučeniny.
Tento způsob používá katalyzátory na bázi kyseliny fosforečné, fixované na pevném nosiči, které jsou schopny upravovat tak, aby produkovaly více etheru.
Dehydratace ethanolu v plynné fázi v přítomnosti katalyzátorů na bázi oxidu hlinitého může poskytnout 95% výtěžek při výrobě ethyletheru..
Toxicita
Může vyvolat podráždění pokožky a očí kontaktem. Kontakt s pokožkou může způsobit jeho vysychání a popraskání. Ether obvykle neproniká kůží, protože se rychle odpaří.
Podráždění očí způsobené etherem je obvykle mírné, v případě silného podráždění je poškození obvykle reverzibilní..
Jeho požití způsobuje narkotické účinky a podráždění žaludku. Těžké požití může způsobit poškození ledvin.
Vdechnutí etheru může způsobit podráždění nosu a krku. V případě vdechnutí etheru může nastat: ospalost, vzrušení, závratě, zvracení, nepravidelné dýchání a zvýšené slinění..
Vysoká expozice může způsobit ztrátu vědomí a dokonce i smrt.
OSHA stanoví limit expozice na pracovišti v průměru 800 ppm v průběhu 8hodinové směny.
Úrovně podráždění očí: 100 ppm (člověk). Úrovně podráždění očí: 1200 mg / m3 (400 ppm).
Použití
Organické rozpouštědlo
Je to organické rozpouštědlo, které se používá k rozpouštění bromu, jodu a dalších halogenů; většina lipidů (tuků), pryskyřic, čistých kaučuků, některých alkaloidů, gum, parfémů, acetátu celulózy, nitrátu celulózy, uhlovodíků a barviv.
Kromě toho se používá při extrakci aktivních látek živočišných tkání a rostlin, protože má nižší hustotu než voda a plave na ní, přičemž požadované látky se rozpouští v etheru..
Celková anestezie
Používá se jako obecné anestetikum od roku 1840, kdy se nahradí chloroform za terapeutickou výhodu. Je to však hořlavá látka, a proto se setkává s těžkými obtížemi při jejím použití v rámci klinického prostředí.
Kromě toho produkuje u pacientů některé nežádoucí pooperační vedlejší účinky, jako je nevolnost a zvracení.
Z těchto důvodů bylo použití etheru jako celkového anestetika vyřazeno a nahrazeno jinými anestetiky, jako je halothan..
Duch éteru
Ether smíchaný s ethanolem byl použit k vytvoření roztoku zvaného duch éteru, který se používá při léčbě nadýmání žaludku a mírnějších forem gastralgie..
Hodnocení krevního oběhu
Ether je používán k hodnocení krevního oběhu mezi paží a paží. Ether se vstřikuje do paže, přivádí krev do pravé síně, pak do pravé komory a odtud do plic..
Doba, která uplyne od vstřikování éteru, až po příjem éterového zápachu ve vydechovaném vzduchu, je přibližně 4 až 6 s.
Výukové laboratoře
Ether je používán v učebních laboratořích v mnoha experimentech; například v ukázce Mendelových zákonů genetiky.
Ether se používá k otupení mouchy rodu Drosophila a umožnění nezbytných křížení mezi nimi, aby se daly doložit zákony genetiky
Odkazy
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organická chemie. Aminy (10)th vydání.). Wiley Plus.
- Carey F. (2008). Organická chemie (Šesté vydání). Mc Graw Hill.
- Sevier. (2018). Diethylether. Science Direct. Zdroj: sciencedirect.com
- Editoři Encyclopaedia Britannica. (2018). Ethylether. Britannica ncyclopædia. Zdroj: britannica.com
- PubChem (2018). Ether. Zdroj: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Diethylether. Zdroj: en.wikipedia.org
- Bezpečnostní list XI: ethylether. [PDF] Obnoveno z: quimica.unam.mx


