Formulace osmolarity, jak ji vypočítat a odlišit od osmolality
osmolarita je parametr, který měří koncentraci chemické sloučeniny v litru roztoku, pokud přispívá ke koligační vlastnosti známé jako osmotický tlak uvedeného roztoku..
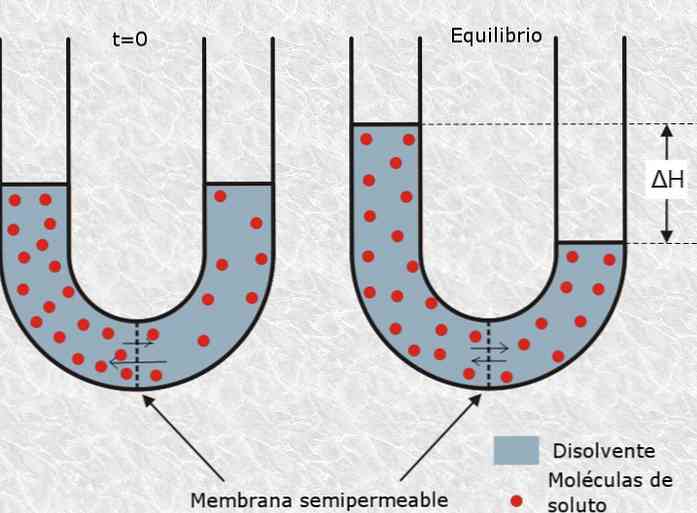
V tomto smyslu osmotický tlak roztoku se týká množství tlaku potřebného pro zpomalení procesu osmózy, který je definován jako selektivní průchod částic rozpouštědla pomocí semipermeabilní nebo porézní membrány z roztoku. nižší koncentrace na koncentrovanější.
Také jednotka, která se používá k vyjádření množství rozpuštěných částic, je osmol (jehož symbolem je Osm), který není součástí Mezinárodního systému jednotek (SI), který se používá téměř v celém světě. Koncentrace rozpuštěné látky v roztoku je definována v jednotkách Osmolů na litr (Osm / l)..
Index
- 1 Vzorec
- 1.1 Definice proměnných ve vzorci osmolarity
- 2 Jak jej vypočítat?
- 3 Rozdíly mezi osmolaritou a osmolalitou
- 4 Odkazy
Vzorec
Jak bylo uvedeno výše, osmolarita (také známá jako osmotická koncentrace) je vyjádřena v jednotkách definovaných jako Osm / l. Je to dáno vztahem ke stanovení osmotického tlaku a měřením difúze rozpouštědla osmózou.
V praxi může být osmotická koncentrace určena jako fyzikální veličina s použitím osmometru.
Osmometer je přístroj používaný při měření osmotického tlaku roztoku, stejně jako stanovení dalších koligačních vlastností (jako je tlak par, zvýšení teploty varu nebo deprese bodu tuhnutí) pro získání hodnoty osmolarity roztoku.
Tímto způsobem se pro výpočet tohoto parametru měření použije následující vzorec, který bere v úvahu všechny faktory, které mohou tuto vlastnost ovlivnit..
Osmolarita = ΣφiniCi
V této rovnici je osmolarita stanovena jako součet vyplývající z násobení všech hodnot získaných ze tří různých parametrů, které budou definovány níže..
Definice proměnných ve vzorci osmolarity
V první řadě se jedná o osmotický koeficient, reprezentovaný řeckým písmenem φ (phi), který vysvětluje, jak daleko se řešení ideálního chování vzdaluje, nebo jinými slovy míra nepřesnosti, kterou se solut projevuje v řešení..
Nejjednodušším způsobem φ se rozumí stupeň disociace solutu, který může mít hodnotu mezi nulou a jednou, kde maximální hodnota jednotky představuje disociaci 100%; to je absolutní.
V některých případech - jako je sacharóza - tato hodnota převyšuje jednotu; zatímco v jiných případech, jako například v případě solí, vliv elektrostatických interakcí nebo sil způsobuje osmotický koeficient s hodnotou menší než je jednota, i když dochází k absolutní disociaci.
Na druhé straně hodnota n označuje množství částic, ve kterých může být molekula disociována. V případě iontových druhů je jako příklad uveden chlorid sodný (NaCl), jehož hodnota n se rovná dvěma; zatímco v neionizované molekule glukózy je hodnota n rovna jedné.
Konečně hodnota c představuje koncentraci rozpuštěné látky, vyjádřenou v molárních jednotkách; a index i označuje identitu specifické rozpuštěné látky, ale musí být stejná při násobení tří výše uvedených faktorů a tím získání osmolarity.
Jak to vypočítat?
V případě iontové sloučeniny KBr (známé jako bromid draselný), pokud máte roztok o koncentraci 1 mol / l KBr ve vodě, má se za to, že má osmolaritu rovnou 2 osmol / l.
Toto je kvůli jeho silnému elektrolytovému charakteru, který favorizuje jeho kompletní disociaci ve vodě a dovolí vydání dvou nezávislých iontů (K \ t+ a Br-), které mají nějaký elektrický náboj, takže každý mol KBr se rovná dvěma osmolům v roztoku.
Analogicky pro roztok s koncentrací 1 mol / l BaCl2 (známý jako chlorid barnatý) ve vodě, má osmolaritu rovnou 3 osmol / l.
Je to proto, že se uvolňují tři nezávislé ionty: Ba ion2+ a dva ionty Cl-. Pak každý mol BaCl2 je ekvivalentní třem osmolům v roztoku.
Na druhé straně neiontové druhy nepodléhají takové disociaci a vznikají jeden osmol pro každý mol rozpuštěné látky. V případě roztoku glukózy o koncentraci 1 mol / l se to rovná 1 osmolu / l roztoku.
Rozdíly mezi osmolaritou a osmolalitou
Osmol je definován jako počet částic, které jsou rozpuštěny v objemu 22,4 1 rozpouštědla, podrobeny teplotě 0 ° C a které způsobují generování osmotického tlaku rovného 1 atm. Je třeba poznamenat, že tyto částice jsou považovány za osmoticky aktivní.
V tomto smyslu vlastnosti známé jako osmolarita a osmolalita se vztahují ke stejnému měření: koncentrace rozpuštěné látky v roztoku nebo, jinak řečeno, obsah celkových částic rozpuštěné látky v roztoku..
Základní rozdíl, který je zjištěn mezi osmolaritou a osmolalitou, je v jednotkách, ve kterých je každý reprezentován:
Osmolarita je vyjádřena v množství látky na objem roztoku (tj. Osmol / l), zatímco osmolalita je vyjádřena v množství látky na hmotnost rozpouštědla (tj. Osmol / kg roztoku)..
V praxi jsou oba parametry používány lhostejným způsobem, dokonce se projevují v různých jednotkách, a to z toho důvodu, že mezi celkovými veličinami různých měření je nedocenitelný rozdíl..
Odkazy
- Wikipedia. (s.f.). Osmotická koncentrace. Zdroj: es.wikipedia.org
- Chang, R. (2007). Chemie, deváté vydání. Mexiko: McGraw-Hill.
- Evans, D. H. (2008). Osmotická a iontová regulace: buňky a zvířata. Citováno z knih.google.co.ve
- Potts, W. T., a Parry, W. (2016). Osmotická a iontová regulace u zvířat. Citováno z knih.google.co.ve
- Armitage, K. (2012). Vyšetřování v obecné biologii. Citováno z knih.google.co.ve


