Struktura, vlastnosti, syntéza, použití a rizika sodíku Benzoát
benzoát sodný je organická sůl, jejíž chemický vzorec je C6H5COONa. Vyrábí se nebo vzniká neutralizační reakcí mezi kyselinou benzoovou a hydroxidem sodným. Výsledkem je bílá pevná látka (spodní obrázek) rozpustná ve vodě a rozkládá se zahřátím na 120 ° C.
Tato sůl se přirozeně vyskytuje v různých druzích zeleniny a ovoce, jako jsou: borůvky, švestky, rozinky, skořice, hřebíček a jablka. Je také metabolitem řas a rostlin.

Benzoát sodný se neakumuluje v těle, protože se rychle spojuje s aminokyselinou glycinem za vzniku kyseliny hippurové, která se volně vylučuje močí.
Tato sloučenina se používá s konzervačním činidlem, jejíž účinek je účinnější při kyselém pH. To je způsobeno přítomností organických kyselin, které dávají potravině pH vhodné pro působení benzoátu sodného; které jako takové končí protonizací na kyselinu benzoovou.
Tato sůl se také používá při léčbě dědičných metabolických poruch močovinového cyklu, které produkují akumulaci intermediárního metabolitu, pro který je enzym, který ho zpracovává, nedostatečný..
Mezinárodní program pro chemickou bezpečnost nezjistil žádné škodlivé účinky benzoanu sodného na člověka, pro spotřebu 647 - 825 mg / kg tělesné hmotnosti..
Bylo však hlášeno, že benzoát sodný může vyvolat pseudoalergické reakce a zhoršit symptomy u pacientů s častými epizodami urtikárie a astmatu..
Index
- 1 Struktura benzoátu sodného
- 2 Vlastnosti
- 2.1 Chemické názvy
- 2.2 Fyzický popis
- 2.3 Vůně
- 2.4 Chuť
- 2.5 Bod vzplanutí
- 2.6 Automatické zapalování
- 2.7 Hustota
- 2.8 Rozpustnost
- 2.9 Stabilita
- 2.10 Rozklad
- 2,11 pH
- 2.12 Povrchové napětí
- 3 Shrnutí
- 4 Použití
- 4.1 V potravinách
- 4.2 Lékařské ošetření
- 4.3 Ostatní
- 5 Rizika
- 6 Odkazy
Struktura benzoátu sodného
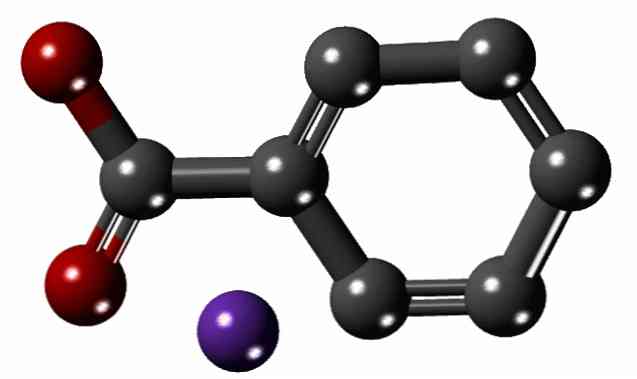
V horním obrázku je struktura benzoátu sodného ukázána na modelu koulí a tyčí. Aromatický kruh může být viděn pouhým okem, s karboxylátovou skupinou, -COO-, spojené s tím (červené koule); a druhá, na oplátku, elektrostaticky přitahuje Na kation+ (fialová koule).
Protože rozdíl ve velikosti mezi oběma ionty je velký (v porovnání s obrázkem), není překvapující, že retikulární energie krystalů benzoátu sodného je nízká. To způsobuje, že jejich krystaly mají přirozenou tendenci solubilizovat se v polárních rozpouštědlech nebo trpět řadou chemických reakcí.
C6H5COO- Může přijímat dva vodíkové mosty ze dvou molekul vody, což podporuje jeho hydrataci. Mezitím Na+ Rovněž končí solvatované vodou, překonává elektrostatické síly, které ho drží společně s C6H5COO-.
Tato sůl se tedy skládá z iontů C6H5COO- a Na+, které jsou uspořádány uspořádaným způsobem pro vytváření krystalů. V literatuře není získána žádná informace o jeho krystalické struktuře, takže není známo, jaký je typ jednotkové buňky pro tuto sůl.
Vlastnosti
Chemické názvy
-Benzoát sodný
-Sodná sůl kyseliny benzoové
-Sobenato
-Antimol.
Fyzický popis
Bílé granule nebo krystalický prášek. Bezbarvý krystalický prášek.
Vůně
WC.
Chuť
Bittersweet, svíravý a nepříjemný.
Bod zapálení
> 100 ° C.
Automatické zapalování
> 500 ° C.
Hustota
1,50 g / cm3.
Rozpustnost
-Rozpustný v kapalném amoniaku a pyridinu.
-Mírně rozpustný v ethanolu: 8,22 g / 100 g při 25 ° C.
-V methanolu je rozpustnější než v ethanolu: 8,22 g / 100 g při 15 ° C.
Stabilita
Je stabilní za doporučených skladovacích podmínek. Může být citlivý na vlhkost, hydrolyzovat na kyselinu benzoovou. Nekompatibilní se silnými oxidačními činidly, zásadami a minerálními kyselinami.
Rozklad
Při zahřátí na teplotu 120 ° C (248 ° F) se uvolňuje ostrý kouř oxidu sodného a dalších složek, které mohou být toxické a karcinogenní.
Při rozkladu při teplotě 120 ° C zabraňuje tomu, aby bylo možno přesně určit jeho teploty varu a teploty tání, přičemž uváděné hodnoty těchto parametrů jsou teoretickými odhady..
pH
V blízkosti 8, rozpuštěné ve vodě. To znamená, že se jedná o bazickou sůl. Je to proto, že hydrolyzuje na uvolňování OH iontů-.
Povrchové napětí
72,9 mN / cm při 20 ° C v roztoku 1 g / l vody.
Syntéza
Kyselina benzoová, která se podílí na syntéze benzoátu sodného, se vyrábí hlavně třemi způsoby:
-Naftalen se oxiduje oxidem vanadičným za vzniku anhydridu kyseliny ftalové. Tato sloučenina může podstoupit dekarboxylaci, aby způsobila kyselinu benzoovou, protože ve své struktuře se dvěma aromatickými kruhy se zdá, že mají dvě skupiny -COO kondenzované dohromady.
-Toluen se oxiduje na kyselinu benzoovou přidáním kyseliny dusičné. V této reakci je methylová skupina "jednoduše" oxidována na karboxylovou skupinu:
C6H5CH3 => C6H5COOH
-A konečně, benzotrichlorid je hydrolyzován působením minerálních kyselin, původní kyseliny benzoové.
Získaná kyselina benzoová se získá některým z těchto tří způsobů, poté se rozpustí v hydroxidu sodném. Tyto sloučeniny podléhají neutralizační reakci za vzniku benzoátu sodného a vody.
C6H5COOH + NaOH => C6H5COONa + H2O
Reakce může být také provedena s uhličitanem sodným, i když jeho výtěžek může být menší, než je žádoucí.
Použití
V potravinách
Benzoan sodný je konzervačním činidlem potravin, které je schopno inhibovat nebo oddálit proces kvašení, okyselení nebo jakýkoli proces, který způsobuje jejich zhoršení. Kromě toho má benzoát sodný fungicidní účinek.
Tato sůl je schopna eliminovat kvasinky, bakterie a houby přítomné v potravinách. Jeho konzervační účinek je účinnější při pH < 6; es decir, en condiciones ácidas. Por esta razón es usado en conservas y en aliños de ensaladas que contienen vinagre (ácido acético).
Benzoát sodný se také používá při konzervaci sycených nápojů a nealkoholických nápojů, ve kterých je přítomna kyselina uhličitá. Také v džemech, bohatých na kyselinu citrónovou, a obecně v potravinách s přítomnými kyselinami, které vytvářejí kyselé prostředí.
Kromě toho se používá v krmivu s koncentrací benzoanu sodného 0,1%. Maximální množství použité kyseliny benzoové a benzoanu sodného, jako konzervačních látek v potravinách, nepřesahuje 2 000 mg / kg potraviny.
Lékařské ošetření
Akutní hyperamonemie
Fenylacetát sodný a benzoát sodný se používají ve formě adjuvantních terapií při léčbě akutní hyperamonémie a související encefalopatie u pacientů se změnami cyklu močoviny..
Tyto sloučeniny jsou klasifikovány jako léčiva pro vzácná onemocnění. Toto označení platí pro drogy, které nejsou z ekonomického hlediska ziskové.
Schizofrenie
Benzoát sodný se experimentálně používá při léčbě schizofrenie. Ústřední částí výzkumu je úloha, kterou při léčbě splňuje inhibice oxidázových enzymů D-aminokyselin, aktivita, která odpovídá benzoátu sodnému.
Arginosukcinová acidurie
Benzoát sodný se používá při léčbě argininosukcinové acidurie, dědičné metabolické poruchy, která může u pacientů způsobit zvýšení koncentrace amoniaku, schopného ovlivnit centrální nervový systém..
Inhibitor
-Je to inhibitor enzymu araquidonato 15-lipoxygenázy, enzymu, který je zkoumán farmaceutickým průmyslem za účelem zapojení do koronárních srdečních onemocnění..
-Inhibuje působení lipázového enzymu triacylglyceridů, enzymu, který působí uvolňování glycerolu a mastných kyselin v tenkém střevě, což umožňuje absorpci těchto lipidů přítomných v potravinách..
Může být možné použít benzoát sodný pro regulaci intestinální absorpce lipidů, jako jsou triacylglyceridy.
Dědičné poruchy
Benzoát sodný se používá při léčbě několika dědičných poruch souvisejících s metabolismem aminokyselin, mezi nimiž jsou zmíněny: léčba hyperergininémie a léčba nedostatku enzymu translokace ornitinu..
Ostatní
-Používá se při oplachování na bázi alkoholu a při leštění stříbra. Kromě toho se používá při zpracování pyrotechnických sloučenin, které jsou zodpovědné za píšťalku vyrobenou při zapálení.
-Používá se jako antikorozní, což je jeden z hlavních požadavků při výrobě této soli. Používá se také v chladivech, nemrznoucích prostředcích a dalších systémech na bázi vody.
-Při formulaci plastů, jako je polypropylen, se používá ke zlepšení jeho pevnosti a jasnosti.
-Slouží jako stabilizátor v koupelnách a fotografických procesech.
Rizika
Benzoát sodný je klasifikován FDA jako "obecně bezpečný" v dávce 0,1% hmotnosti potraviny. Není považován za dráždivý pro kontakt s pokožkou a očima, takže lze říci, že akutní toxicita je nízká.
Benzoát sodný však může způsobit neimunologické reakce (pseudoalergie) kontaktem. Tento účinek je vzácný u normálních lidí, ale u pacientů s častými epizodami urtikárie nebo symptomů astmatu může dojít ke zvýšení četnosti těchto příznaků..
Ve studiích na potkanech a myších nebyly nalezeny žádné známky karcinogenního účinku benzoátu sodného.
Bylo poukázáno na nepříjemnosti jeho použití v přítomnosti kyseliny askorbové, která by mohla produkovat benzen; toxická sloučenina označená jako karcinogenní.
Odkazy
- Net Industries. (2019). Produkce benzoátu sodného. Citováno z: science.jrank.org
- Wikipedia. (2019). Benzoát sodný. Zdroj: en.wikipedia.org
- PubChem. (2019). Benzoát sodný. Zdroj: pubchem.ncbi.nim.nih.gov
- Hanes T. (2019). Fakta o benzoátu sodném. Livestrong. Zdroj: livestrong.com
- Chemická kniha. (2017). Benzoát sodný. Zdroj: chemicalbook.com
- Lane H. a kol. (2013) Jama Psichiatry. 70 (12): 1267 - 1275.
- Světová zdravotnická organizace Ženeva. (12. dubna 2005). Kyselina benzoová a benzoát sodný. [PDF] Zdroj: who.int


