Biologický výkon katalyzátoru a příklady
A biologický katalyzátor o biokatalyzátor je molekula, obecně proteinového původu, která má schopnost urychlit chemické reakce, které se vyskytují uvnitř živých bytostí. Molekuly katalytického proteinu jsou enzymy a molekuly RNA jsou ribozymy. V tomto článku se zaměříme na zkoumání enzymů, které jsou nejznámějšími biologickými katalyzátory.
V nepřítomnosti enzymů nemohlo dojít k obrovskému počtu reakcí, ke kterým dochází v buňce a které umožňují život. Ty jsou zodpovědné za urychlení procesu v řádu řádů blízkých 106 - av některých případech mnohem větší.
Index
- 1 Katalýza
- 2 Enzymy
- 2.1 Co je enzym?
- 2.2 Charakteristika enzymů
- 2.3 Nomenklatura a klasifikace enzymů
- 2.4 Jak enzymy fungují?
- 2.5 Enzymatické inhibitory
- 2.6 Příklady
- 3 Rozdíl mezi biologickými katalyzátory (enzymy) a chemickými katalyzátory
- 3.1 Reakce katalyzované enzymy se vyskytují rychleji
- 3.2 Většina enzymů pracuje za fyziologických podmínek
- 3.3 Specifičnost
- 3.4 Enzymatická regulace je přesná
- 4 Odkazy
Katalýza
Katalyzátorem je molekula schopná měnit rychlost chemické reakce, aniž by byla při uvedené reakci spotřebována.
Chemické reakce zahrnují energii: počáteční molekuly zapojené do reakce nebo reaktanty začínají se stupněm energie. Další množství energie je absorbováno k dosažení "přechodného stavu". Následně je s produkty uvolněna energie.
Rozdíl energie mezi reaktanty a produkty je vyjádřen jako AG. Pokud jsou energetické hladiny produktů vyšší než reaktanty, je reakce endergní a není spontánní. Naopak, pokud je energie produktů nižší, reakce je exergonická a spontánní.
Pokud je však reakce spontánní, neznamená to, že k ní dojde při znatelné rychlosti. Rychlost reakce závisí na ΔG * (hvězdička označuje aktivační energii).
Čtenář musí mít tyto pojmy na paměti, aby pochopil, jak funguje enzymy.
Enzymy
Co je to enzym?
Enzymy jsou biologické molekuly neuvěřitelně složité, skládající se především z proteinů. Proteiny jsou zase dlouhými řetězci aminokyselin.
Jednou z nejvýraznějších vlastností enzymů je jejich specificita v cílové molekule - tato molekula se nazývá substrát.
Charakteristika enzymů
Enzymy existují v několika formách. Některé se skládají výhradně z bílkovin, zatímco jiné mají nebílkovinné oblasti zvané kofaktory (kovy, ionty, organické molekuly atd.).
Apoenzym je tedy enzym bez kofaktoru a kombinace apoenzymu a jeho kofaktoru se nazývá holoenzym.
Jsou to molekuly značně velké velikosti. Avšak pouze malé místo enzymu se přímo účastní reakce se substrátem a tato oblast je aktivním místem.
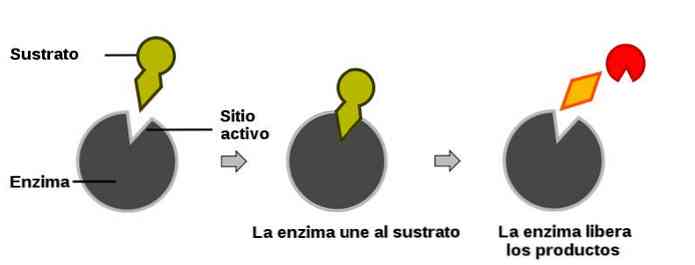
Když reakce začne, enzym je spojen se svým substrátem, protože klíč je spojen s jeho zámkem (tento model je zjednodušením skutečného biologického procesu, ale slouží k ilustraci procesu)..
Všechny chemické reakce, které se vyskytují v našem těle, jsou katalyzovány enzymy. Kdyby tyto molekuly neexistovaly, museli bychom čekat stovky nebo tisíce let, než se reakce dokončí. Regulace enzymatické aktivity musí být proto řízena velmi specifickým způsobem.
Nomenklatura a klasifikace enzymů
Když vidíme molekulu, jejíž název končí v -ase, můžeme si být jisti, že se jedná o enzym (i když existují výjimky z tohoto pravidla, jako je trypsin). Toto je úmluva pro označení názvu enzymů.
Existuje šest základních typů enzymů: oxidoreduktázy, transferázy, hydrolázy, lyázy, izomerázy a ligázy; zodpovědný za: redoxní reakce, přenos atomů, hydrolýza, přidání dvojných vazeb, izomerizace a vazba molekul.
Jak enzymy fungují?
V sekci o katalýze jsme uvedli, že rychlost reakce závisí na hodnotě ΔG *. Čím vyšší je tato hodnota, tím pomalejší a pomalejší reakce. Enzym je zodpovědný za snížení uvedeného parametru - čímž se zvyšuje rychlost reakce.
Rozdíl mezi produkty a reaktanty zůstává identický (enzym ho neovlivňuje), stejně jako distribuce stejného produktu. Enzym usnadňuje tvorbu přechodového stavu.
Inhibitory enzymů
V kontextu studia enzymů jsou inhibitory látky, které dokáží snížit aktivitu katalyzátoru. Jsou klasifikovány do dvou typů: kompetitivních a nekompetitivních inhibitorů. Ti prvního typu soutěží se substrátem a ostatní ne.
Obecně je inhibiční proces reverzibilní, i když některé inhibitory mohou zůstat s enzymem téměř trvale vázány.
Příklady
V našich buňkách je velké množství enzymů - a v buňkách všech živých bytostí. Nejznámější jsou však ty, které se mimo jiné účastní metabolických drah, jako je glykolýza, Krebsův cyklus, elektronový transportní řetězec..
Sukcinátdehydrogenáza je enzym typu oxidoreduktázy, který katalyzuje oxidaci sukcinátu. V tomto případě reakce zahrnuje ztrátu dvou atomů vodíku.
Rozdíl mezi biologickými katalyzátory (enzymy) a chemickými katalyzátory
Existují katalyzátory chemické povahy, které, podobně jako biologické, zvyšují rychlost reakcí. Existují však značné rozdíly mezi oběma typy molekul.
Enzymem katalyzované reakce probíhají rychleji
Nejprve se enzymům podaří zvýšit rychlost reakcí v řádu řádů blízkých 106 až 1012. Chemické katalyzátory také zvyšují rychlost, ale jen několik řádů.
Většina enzymů pracuje za fyziologických podmínek
Protože biologické reakce probíhají uvnitř živých bytostí, jejich optimální podmínky obklopují fyziologické hodnoty teploty a pH. Chemici naopak potřebují drastické podmínky teploty, tlaku a kyselosti.
Specifičnost
Enzymy jsou velmi specifické v reakcích, které katalyzují. Ve většině případů pracují pouze s jedním substrátem nebo s několika substráty. Specifičnost se rovněž vztahuje na typ výrobků, které vyrábějí. Rozsah substrátů chemických katalyzátorů je mnohem širší.
Síly, které určují specifičnost interakce mezi enzymem a jeho substrátem, jsou stejné, které určují konformaci stejného proteinu (Van der Waalsovy interakce, elektrostatické vazby, vodíkové vazby a hydrofobní)..
Enzymatická regulace je přesná
Nakonec mají enzymy větší schopnost regulace a jejich aktivita se liší v závislosti na koncentraci různých látek v buňce.
Mezi regulačními mechanismy najdeme alosterickou kontrolu, kovalentní modifikaci enzymů a variace v množství syntetizovaného enzymu..
Odkazy
- Berg, J. M., Stryer, L., & Tymoczko, J. L. (2007). Biochemie. Obrátil jsem se.
- Campbell, M. K., & Farrell, S. O. (2011). Biochemie Šesté vydání. Thomson. Brooks / Cole.
- Devlin, T. M. (2011). Učebnice biochemie. John Wiley & Sons.
- Koolman, J., & Röhm, K. H. (2005). Biochemie: text a atlas. Panamericana Medical.
- Mougios, V. (2006). Cvičení biochemie. Lidská kinetika.
- Müller-Esterl, W. (2008). Biochemie Základy medicíny a biologických věd. Obrátil jsem se.
- Poortmans, J.R. (2004). Principy cvičení biochemie. Karger.
- Voet, D., & Voet, J. G. (2006). Biochemie. Panamericana Medical.


