Oxidy dusíku (NOx) Různé formulace a názvosloví
oxidy dusíku jsou to v podstatě plynné anorganické sloučeniny, které obsahují vazby mezi atomy dusíku a kyslíku. Jeho chemický vzorec je NOx, indikující, že oxidy mají různé podíly kyslíku a dusíku.
Dusík vede skupinu 15 periodické tabulky, zatímco kyslíková skupina 16; oba elementy jsou členy období 2. Tato blízkost je důvod proč N-O vazby jsou kovalentní v oxidech. Tímto způsobem jsou vazby v oxidech dusíku kovalentní.
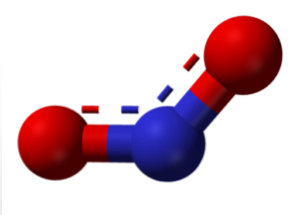
Všechny tyto vazby lze vysvětlit pomocí teorie molekulárního orbitálu, který odhaluje paramagnetismus (elektron nepárovaný v posledním molekulárním orbitálu) některých těchto sloučenin. Nejběžnějšími sloučeninami jsou oxid dusnatý a oxid dusičitý.
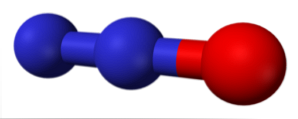
Molekula v horním obrázku odpovídá úhlové struktuře v plynné fázi oxidu dusičitého (NO2). Oproti tomu má oxid dusnatý (NO) lineární strukturu (s ohledem na sp hybridizaci obou atomů).
Oxidy dusíku jsou plyny produkované mnoha lidskými činnostmi, od řízení vozidla nebo kouření cigaret po průmyslové procesy jako znečišťující odpad. NO je však přirozeně produkován enzymatickými reakcemi a bleskem v bouřkách: N2(g) + O2(g) => 2NO (g)
Vysoké teploty paprsků rozbíjejí energetickou bariéru, která brání této reakci v normálních podmínkách. Jaká energetická bariéra? Ten, který tvoří trojná vazba N bondN, tvoří N-molekulu2 inertní plyn z atmosféry.
Index
- 1 Oxidační čísla pro dusík a kyslík v jejich oxidech
- 2 Různé formulace a názvosloví
- 2.1 Oxid dusný (N2O)
- 2.2 Oxid dusnatý (NO)
- 2.3 Oxid dusnatý (N2O3)
- 2.4 Dioxid a oxid dusnatý (NO2, N2O4)
- 2.5 Oxid dusný (N2O5)
- 3 Odkazy
Oxidační čísla pro dusík a kyslík v jejich oxidech
Elektronická konfigurace kyslíku je [He] 2s22p4, potřebovat jen dva elektrony dokončit oktet jeho valence shell; to znamená, že může získat dva elektrony a mít oxidační číslo rovné -2.
Na druhé straně, elektronická konfigurace pro dusík je [He] 2s22p3, být schopný získat až tři elektrony k naplnění jeho valence oktet; například v případě amoniaku (NH3) má oxidační číslo rovné -3. Ale kyslík je mnohem více elektronegativní než vodík a "nutí" dusík, aby sdílel své elektrony.
Kolik elektronů může dusík sdílet s kyslíkem? Pokud sdílíte elektrony vaší valenční skořepiny jeden po druhém, dosáhnete limitu pěti elektronů, což odpovídá oxidačnímu číslu +5.
V závislosti na tom, kolik vazeb tvoří kyslík, se oxidační čísla dusíku pohybují od +1 do +5.
Různé formulace a názvosloví
Oxidy dusíku ve vzrůstajícím počtu oxidačních čísel dusíku jsou:
- N2Nebo oxid dusný (+1)
- NO, oxid dusnatý (+2)
- N2O3, oxid dusičitý (+3)
- NE2, oxid dusičitý (+4)
- N2O5, oxid dusný (+5)
Oxid dusný (N2O)
Oxid dusný (nebo populárně známý jako smích plyn) je bezbarvý plyn, s mírnou sladkou vůní a málo reaktivní. Může být vizualizován jako N molekula2 (modré koule), který na jednom konci přidal atom kyslíku. Připravuje se tepelným rozkladem dusičnanových solí a používá se jako anestetikum a analgetikum.
Dusík má oxidační číslo +1 v tomto oxidu, což znamená, že není příliš oxidován a jeho poptávka po elektronech není přesvědčivá; musíte však získat pouze dva elektrony (jeden pro každý dusík), aby se stal stabilním molekulárním dusíkem.
V zásaditých a kyselých roztocích jsou tyto reakce:
N2O (g) + 2H+(ac) + 2e- => N2(g) + H2O (l)
N2O (g) + H2O (l) + 2e- => N2(g) + 2OH-(ac)
Tyto reakce, i když termodynamicky, jsou podporovány tvorbou stabilní molekuly N2, vyskytují se pomalu a činidla, která darují pár elektronů, musí být velmi silná redukční činidla.
Oxid dusnatý (NO)
Tento oxid se skládá z bezbarvého, reaktivního a paramagnetického plynu. Stejně jako oxid dusný, má lineární molekulární strukturu, ale s velkým rozdílem, že vazba N = O má také charakter trojné vazby..
NO se rychle oxiduje ve vzduchu za vzniku NO2, a tak generují stabilnější molekulární orbitály s více oxidovaným atomem dusíku (+4).
2NO (g) + O2(g) => 2NO2(g)
Biochemické a fyziologické studie jsou v pozadí benigní role tohoto oxidu v živých organismech.
To nemůže tvořit N-N vazby s jinou molekulou NO kvůli delokalizaci nepárového elektronu v molekulárním orbitálu, který je nasměrován více k atomu kyslíku (kvůli jeho vysoké electronegativity). Opak se vyskytuje u NO2, které mohou tvořit plynné dimery.
Oxid dusnatý (N2O3)
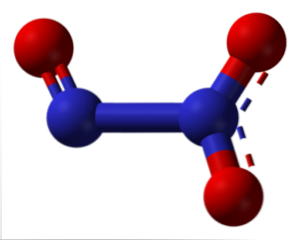
Tečkované čáry struktury ukazují rezonanci dvojné vazby. Stejně jako všechny atomy mají sp hybridizaci2, molekula je plochá a molekulární interakce jsou dostatečně účinné, aby oxid dusnatý existoval jako modrá pevná látka pod -101 ° C. Při vyšších teplotách se taví a disociuje na NO a NO2.
Proč je disociovaná? Vzhledem k tomu, že oxidační čísla +2 a +4 jsou stabilnější než +3, jsou tyto oxidy přítomny v oxidech pro každý ze dvou atomů dusíku. To lze opět vysvětlit stabilitou molekulárních orbitálů vyplývajících z disproporce.
Na obrázku vlevo od N2O3 odpovídá NO, zatímco pravá strana NO2. Logicky se vyrábí spojením předchozích oxidů při velmi nízkých teplotách (-20 ° C). N2O3 je anhydrid kyseliny dusité (HNO)2).
Dioxid a oxid dusnatý (NO2, N2O4)
NE2 je to hnědý nebo hnědý plyn, reaktivní a paramagnetický. Protože má nepárový elektron, dimerizuje (váže se) s jinou NO plynnou molekulou2 za vzniku oxidu dusnatého, bezbarvého plynu, který vytváří rovnováhu mezi oběma chemickými druhy:
2NO2(g) <=> N2O4(g)
Jedná se o jedovaté a univerzální oxidační činidlo, které je schopno disproporcionovat v redox reakcích v iontech (oxoanionech).2- a NO3- (generování kyselého deště), nebo v NO.
Podobně NO2 se podílí na komplexních atmosférických reakcích, které způsobují změny koncentrací ozonu (OR3) na pozemních úrovních a ve stratosféře.
Oxid dusný (N2O5)
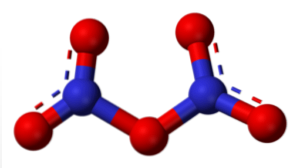
Při hydrataci vytváří HNO3, a při vyšších koncentracích kyseliny je kyslík hlavně protonován s částečným kladným nábojem -O+-H, urychlení redox reakcí
Odkazy
- zeptat seIITI. ((2006–2018)). zeptat seIITI. Získáno dne 29. března 2018, od askIITians: askiitians.com
- Encyclopaedia Britannica, Inc. (2018). Encyclopaedia Britannica. Získaný 29. března 2018, od Encyclopaedia Britannica: britannica.com
- Tox Town. (2017). Tox Town. Získaný 29. března 2018, z Tox Town: toxtown.nlm.nih.gov
- Profesorka Patricia Shapleyová. (2010). Oxidy dusíku v atmosféře. Univerzita Illinois. Získáno dne 29. března 2018, z: butane.chem.uiuc.edu
- Shiver a Atkins. (2008). Anorganická chemie In Prvky skupiny 15. (Čtvrté vydání, str. 361-366). Mc Graw Hill