Chemická struktura propylenu, vlastnosti a použití
propylenu nebo propen při pokojové teplotě a při atmosférickém tlaku je v plynném stavu a stejně jako ostatní alkeny je bezbarvý. Má zápach podobný oleji, ale méně intenzivní. To má dipólový moment protože, ačkoli to postrádá silné polární spojení, jeho molekula je asymetrická.
Rovněž propylen je strukturním izomerem cyklopropanu (mají stejný chemický vzorec C).3H6). Vyskytuje se v přírodě jako důsledek vegetačních a fermentačních procesů. Uměle se vyskytuje při zpracování fosilních paliv, jako je ropa, zemní plyn a v menší míře uhlík.

Podobně ethylen a propylen jsou produkty rafinace ropy v procesu štěpení velkých uhlovodíkových molekul za vzniku malých uhlovodíků ve vysoké poptávce..
Propylen lze také získat použitím různých metodik:
- Reakce reverzibilně ethylenu a butenu, kde jsou dvojné vazby rozbité a přeformulovány za vzniku propylenu.
- Proces dehydrogenace (ztráta vodíku) propanu.
- Jako součást programu výroby olefinů z methanolu (MTO) byl propylen vyroben z methanolu. Ten prošel zeolitovým katalyzátorem, který podporuje jeho dehydrataci a vede k tvorbě ethylenu a propylenu.
3CH3OH (methanol) => CH3CH = CH2 (propylen) + 3H2O (voda)
Index
- 1 Chemická struktura
- 2 Vlastnosti
- 2.1 Molekulová hmotnost
- 2.2 Bod varu
- 2.3 Bod tání
- 2.4 Bod vzplanutí
- 2.5 Rozpustnost
- 2.6 Rozpustnost vyjádřená jako hmotnost
- 2.7 Hustota
- 2.8 Hustota par
- 2.9 Tlak par
- 2.10 Autoignition
- 2.11 Viskozita
- 2.12 Teplo spalování
- 2.13 Teplo odpařování
- 2.14 Povrchové napětí
- 2.15 Polymerizace
- 2.16 Bod tuhnutí
- 2.17 Prahová hodnota zápachu
- 3 Použití
- 3.1 Polypropylen
- 3.2 Acrylonitril
- 3.3 Propylenoxid
- 3.4 Pro syntézu alkoholů a jiných použití
- 4 Odkazy
Chemická struktura
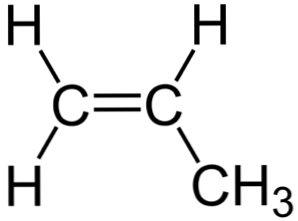
Na obrázku nahoře je vidět chemická struktura propylenu, ve které vyniká asymetrie (pravá strana je odlišná zleva). Jeho uhlíkový skelet, bez atomů H, lze pozorovat jako bumerang.
Tento bumerang představuje nenasycenost nebo dvojnou vazbu na jedné ze svých stran (C1), a proto je plochá v důsledku sp hybridizace2 atomů uhlíku.
Druhá strana je však obsazena methylovou skupinou (-CH3), jejíž hybridizace je sp3 a má tetrahedrální geometrii. Při pohledu zepředu je tedy bumerang plochý s atomy H vyčnívajícími z tohoto úhlu přibližně 109,5 °.
V plynné fázi molekula interaguje slabě s ostatními rozptylovými silami. Interakce mezi dvojnými vazbami (n-n) dvou molekul propylenu je také zabráněno methylovou skupinou.
To má za následek pokles jejich intermolekulárních sil, což se odráží v jejich fyzikálních vlastnostech. Pouze při velmi nízkých teplotách může propylen zaujmout pevnou strukturu, ve které boomeran zůstává ve skupině se svými slabými interakcemi.
Vlastnosti
Jedná se o bezbarvý plyn s aromatickou vůní. Přepravuje se ve formě zkapalněného plynu, a když uniká z kontejnerů, které ho obsahují, ve formě plynu nebo kapaliny. Při nízkých koncentracích vytváří se vzduchem výbušnou a hořlavou směs, jejíž hustota je vyšší než hustota vzduchu.
Molekulová hmotnost
42,081 g / mol
Bod varu
53,9 ° F až 760 mmHg
48 ° C až 760 mmHg
Teplota tání
301,4 ° F
185 ° C
Bod vzplanutí
162 ° F
Rozpustnost
44,6 ml / 100 ml ve vodě.
1,250 ml / 100 ml v ethanolu.
524,5 ml / 100 ml v kyselině octové.
Rozpustnost vyjádřená jako hmotnost
200 mg / l 25 ° C
Hustota
0,609 mg / ml při -52,6 ° F
0,5139 při 20 ° C
Hustota par
1,46 až 32 ° F (vztaženo na vzduch jako referenční).
1,49 (vzduch = 1).
1,91 kg / m3 až 273,15 ° K
Tlak páry
1 mmHg při -205,4 ° F
760 mmHg až -53,9 ° F
8,69 × 103 mmHg při 25 ° C (extrapolovaná hodnota).
1,158 kPa při 25 ° C
15,4 atm při 37 ° C
Autoignition
851 ° F
455 ° C
Viskozita
83,4 mikropoise při 16,7 ° C.
Teplo spalování
16 692 BTU / lb
10,940 cal / g
Odpařovací teplo
104,62 cal / g (při teplotě varu)
Povrchové napětí
16,7 dyn / cm při 90 ° C
Polymerizace
Polymeruje při vysokých teplotách a vysokém tlaku v přítomnosti katalyzátorů.
Bod tuhnutí
185,25 ° C.
Prahová hodnota zápachu
10-50 mg / m3 (detekce)
100 mg / m3 (uznání)
Použití

Používá se v petrochemickém průmyslu jako palivo a alkylační činidlo. V chemickém průmyslu se používá jako surovina pro výrobu a syntézu mnoha derivátů.
Má využití zejména při výrobě polypropylenu, akrylonitrilu (ACN), propylenoxidu (PO), alkoholů, kumenu a akrylových kyselin..
Polypropylen
Polypropylen je jedním z hlavních plastových materiálů s použitím v elektronice a elektrickém příslušenství, vybavení pro domácnost, uzávěry lahví a kufry.
Laminovaný materiál se používá při balení cukrovinek, etiket, CD apod., Zatímco vlákna jsou vyrobena ze složek a oděvů..
Akrylonitril
Elastomerní polymery a vlákna se získávají z akrylonitrilu. Tato vlákna jsou určena pro výrobu různých forem oblečení, jako jsou svetry, ponožky a sportovní oblečení. Používají se také v domácím nábytku, ve složkách, čalounění, polštářích a přikrývkách.
Propylenoxid
Propylenoxid je součástí syntézy polyuretanu. To se používá při výrobě pružné pěny a tuhé pěny. Pružná pěna se používá jako výplň pro domácí nábytek a automobilový průmysl.
Na druhé straně se jako stavební izolační materiál používá hlavně tuhá pěna.
Kromě toho se při výrobě propylenglykolu používá propylenoxid. Tato sloučenina se používá při výrobě nenasycených polyesterových pryskyřic a jako prostředek proti zamrzání.
Dále se při výrobě propylenglykoletheru používá propylenoxid. Tento ether má uplatnění při výrobě barev, oděvů, inkoustů, pryskyřic a čisticích prostředků.
Pro syntézu alkoholů a jiných použití
Propylen umožňuje získání některých alkoholů, mezi nimi isopropanolu, který se používá jako rozpouštědlo v kosmetice a výrobcích pro osobní péči. Kromě toho plní funkci antiseptického činidla.
- Isopropanol se zabývá výrobou barev, pryskyřic, inkoustů a lepicích pásek. Používá se také ve farmaceutickém průmyslu.
- Oxo-alkohol2-ethylhexanol se používá při výrobě ftalátů, změkčovadel, adhezivních materiálů a nátěrových hmot..
- Butanol se používá při výrobě barev, nátěrů, pryskyřic, barviv, léčiv a polymerů.
Na druhé straně se kumen vyrábí z kombinace propylenu a benzenu. Cumene je hlavní složkou při výrobě fenolu a acetonu, který se používá v různých výrobcích, jako jsou polykarbonáty, fenolové pryskyřice, epoxidové pryskyřice a methylmethakrylát..
Nakonec se kyselina akrylová - další produkt odvozený od propylenu - používá při výrobě akrylových esterů a pryskyřic pro nátěry, nátěry a aplikace lepidel..
Odkazy
- Michal Osmenda (26. prosince 2007). Zapál mi oheň. [Obrázek] Získáno 23. května 2018, z: commons.wikimedia.org
- Skupina Linde. (2018). Propylen Získáno dne 23. května 2018, z: linde-gas.com
- Wikipedia. (2018). Propen Získáno dne 23. května 2018, z: en.wikipedia.org
- PubChem. (2018). Propylen Získáno 27. května 2018, z: pubchem.ncbi.nlm.nih.gov
- Vesovic Velisa. (7. února 2011). Propylen Získáno 27. května 2018, z: thermopedia.com
- Jeffrey S. Plotkin. (08.8.2016). Propylene Quandary. Získáno 27. května 2018, od: acs.org
- ICIS. (6. listopadu 2017). Použití propylenu a tržní data. Získáno 27. května 2018, z: icis.com


