Struktura, vlastnosti, rizika a použití vápníku
hydrogenuhličitanu vápenatého je anorganická sůl s chemickým vzorcem Ca (HCO)3)2. Vzniká v přírodě z uhličitanu vápenatého přítomného ve vápencových horninách a minerálech, jako je vápenec.
Uhličitan vápenatý je rozpustnější ve vodě než uhličitan vápenatý. Tato charakteristika umožnila vznik krasových systémů ve vápencových skalách a ve struktuře jeskyní.

Podzemní vody, které procházejí prasklinami, se při vytěsňování oxidu uhličitého (CO) nasycují2). Tyto vody erodují vápencové horniny uvolňující uhličitan vápenatý (CaCO)3), který bude tvořit hydrogenuhličitan vápenatý, podle následující reakce:
CaCO3(s) + CO2(g) + H2O (l) => Ca (HCO)3)2(aq)
K této reakci dochází v jeskyních, kde vzniká velmi tvrdá voda. Hydrogenuhličitan vápenatý se nenachází v pevném stavu, ale ve vodném roztoku spolu s Ca2+, hydrogenuhličitan (HCO)3-) a uhličitanového iontu (CO32-).
Následně, když se sníží saturace oxidu uhličitého ve vodě, dochází k reverzní reakci, to znamená k přeměně hydrogenuhličitanu vápenatého na uhličitan vápenatý:
Ca (HCO)3)2(aq) => CO2 (g) + H2O (l) + CaCO3 (s)
Uhličitan vápenatý je špatně rozpustný ve vodě, což způsobuje jeho srážení jako pevné látky. Výše uvedená reakce je velmi důležitá při tvorbě krápníků, stalagmitů a dalších speleotémů v jeskyních.
Tyto skalní struktury jsou tvořeny kapkami vody, které padají ze stropu jeskyní (horní obraz). CaCO3 přítomné v kapkách vody krystalizují za vzniku uvedených struktur.
Skutečnost, že hydrogenuhličitan vápenatý se nenachází v pevném stavu, způsobila, že jeho použití bylo obtížné a bylo nalezeno několik příkladů. Je také obtížné najít informace o jeho toxických účincích. Tam je zpráva souboru vedlejších účinků jeho použití jako léčba k prevenci osteoporózy.
Struktura
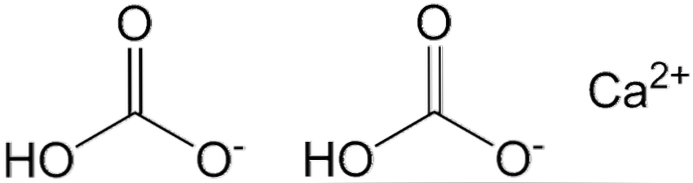
Na horním obrázku jsou zobrazeny dva anionty HCO3- a Ca kation2+ elektrostaticky. Ca2+ podle obrázku by měl být umístěn uprostřed, protože to je to, jak HCOs3- nebudou se navzájem odrazovat kvůli jejich záporným poplatkům.
Záporný náboj v HCO3- je delokalizován mezi dvěma atomy kyslíku rezonancí mezi karbonylovou skupinou C = O a vazbou C-O-; v CO32-, Toto je delocalized mezi třemi atomy kyslíku, protože C-OH vazba je deprotonated a moci proto přijímat záporný náboj resonance \ t.
Geometrie těchto iontů mohou být považovány za koule vápníku obklopené plochými trojúhelníky karbonátů s hydrogenovaným koncem. Co se týče poměru velikosti, vápník je znatelně menší než ionty HCO3-.
Vodné roztoky
Ca (HCO)3)2 To nemůže tvořit krystalické pevné látky, a to opravdu sestává z vodných roztoků této soli. V nich ionty nejsou samy o sobě, jako na obrázku, ale obklopené molekulami H.2O.
Jak se ovlivňují? Každý ion je obklopen hydratační koulí, která bude záviset na kovu, polaritě a struktuře rozpuštěných druhů.
Ca2+ koordinuje s atomy kyslíku vody za vzniku aquokomplexu, Ca (OH)2)n2+, kde n je obecně považováno za šest; to znamená "vodný oktaedron" kolem vápníku.
Zatímco HCO anionty3- s vodíkovými vazbami (OR)2CO-H-OH2) nebo s vodíkovými atomy ve vodě ve směru záporných delokalizací náboje (HOCO)2- H-OH, interakce dipól-ion).
Tyto interakce mezi Ca2+, HCO3- a voda je tak účinná, že činí hydrogenuhličitan vápenatý velmi rozpustným v tomto rozpouštědle; na rozdíl od CaCO3, ve kterém elektrostatické atrakce mezi Ca2+ a CO32- jsou velmi silné, sráží se z vodného roztoku.
Kromě vody existují molekuly CO2 , které reagují pomalu, aby poskytly více HCO3- (v závislosti na hodnotách pH).
Hypotetická pevná látka
Velikost a náboj iontů v Ca (HCO)3)2, ani přítomnost vody, vysvětlit, proč tuhá sloučenina neexistuje; tj. čisté krystaly, které lze charakterizovat rentgenovou krystalografií.3)2 není nic víc než ionty přítomné ve vodě, z níž kavernózní formace nadále rostou.
Ano Ca2+ a HCO3- mohou být izolovány z vody, aby se zabránilo následující chemické reakci:
Ca (HCO)3)2(aq) → CaCO3(s) + CO2(g) + H2O (l)
Pak by mohly být seskupeny do bílé krystalické pevné látky se stechiometrickými podíly 2: 1 (2HCO)3/ 1Ca). Neexistují žádné studie o jeho struktuře, ale mohlo by být srovnáno s NaHCO3 (pro hydrogenuhličitan hořečnatý, Mg (HCO))3)2, ani neexistuje jako pevná látka), ani s CaCO3.
Stabilita: NaHCO3 vs Ca (HCO)3)2
NaHCO3 Krystalizuje v monoklinickém systému a CaCO3 v trigonálních (kalcitových) a ortorombických (aragonitových) systémech. Pokud byl Na nahrazen+ pro Ca2+, krystalická síť by byla destabilizována větším rozdílem ve velikostech; to je Na+ protože je menší, tvoří s HCO stabilnější krystal3- ve srovnání s Ca2+.
Ve skutečnosti, Ca (HCO)3)2(aq) potřebuje vodu, aby se odpařila, takže její ionty mohou být seskupeny do krystalu; ale krystalická mřížka tohoto není dostatečně silná, aby to při pokojové teplotě. Když se voda ohřívá, dochází k rozkladu (výše uvedená rovnice).
Být Na iontem+ v roztoku by to vytvořilo krystal s HCO3- před jeho tepelným rozkladem.
Důvodem proč Ca (HCO)3)2 nezkrystalizuje (teoreticky), to je rozdílem iontových poloměrů nebo velikostí jeho iontů, které nemohou tvořit stabilní krystal před jeho rozkladem.
Ca (HCO)3)2 vs CaCO3
Na druhé straně byl přidán H+ krystalické struktury CaCO3, drasticky by změnily své fyzikální vlastnosti. Možná, že jeho teploty tání značně poklesnou a dokonce i morfologie krystalů skončí.
Stojí za to vyzkoušet syntézu Ca (HCO)3)2 pevné? Obtíže mohou překročit očekávání a sůl s nízkou strukturální stabilitou nemusí poskytovat významné dodatečné přínosy v žádném případě, kdy se již používají jiné soli..
Fyzikální a chemické vlastnosti
Chemický vzorec
Ca (HCO)3)2
Molekulová hmotnost
162,11 g / mol
Fyzikální stav
Nezobrazuje se v pevném stavu. Nachází se ve vodném roztoku a pokusy o jeho přeměnu na pevnou látku odpařením vody, nepracovaly, protože se přeměňují na uhličitan vápenatý.
Rozpustnost ve vodě
16,1 g / 100 ml při 0 ° C; 16,6 g / 100 ml při 20 ° C a 18,4 g / 100 ml při 100 ° C. Tyto hodnoty svědčí o vysoké afinitě molekul vody pro ionty Ca (HCO)3)2, jak je vysvětleno v předchozí části. Mezitím, pouze 15 mg CaCO3 rozpouštějí se v litru vody, což odráží jejich silné elektrostatické interakce.
Protože Ca (HCO)3)2 nemůže tvořit pevnou látku, její rozpustnost nelze stanovit experimentálně. Vzhledem k podmínkám vytvořeným CO2 rozpuštěná ve vodě obklopující vápenec by mohla být vypočtena hmotnost vápníku rozpuštěného při teplotě T; hmotnost, která by se rovnala koncentraci Ca (HCO)3)2.
Při různých teplotách se rozpuštěná hmota zvyšuje, jak je ukázáno na hodnotách při 0, 20 a 100 ° C. Podle těchto experimentů se tedy stanoví, kolik Ca (HCO) je určeno3)2 se rozpouští v blízkosti CaCO3 ve vodném médiu zplyňovaném CO2. Jakmile unikne CO2 plynný, CaCO3 se vysráží, ale ne Ca (HCO)3)2.
Fúze a body varu
Krystalická síť Ca (HCO)3)2 je mnohem slabší než CaCO3. Jestliže to může být získáno v pevném stavu, a změřit teplotu u kterého to roztaví uvnitř fusiometer, to by jistě dostalo hodnotu hluboko pod 899 ° C. Stejně tak by se dalo očekávat při stanovení teploty varu.
Bod spalování
Není hořlavý.
Rizika
Protože tato sloučenina neexistuje v pevné formě, je nepravděpodobné, že by představovala riziko manipulace s jejími vodnými roztoky, protože jak Ca2+ jako HCO3- nejsou škodlivé při nízkých koncentracích; a proto by největší riziko, že by bylo takové řešení přijímat, by mohlo být způsobeno pouze nebezpečnou dávkou požitého vápníku.
Pokud sloučenina tvoří pevnou látku, i když může být fyzicky odlišná od CaCO3, jeho toxické účinky nesmí přesahovat jednoduché nepohodlí a resekce po fyzickém kontaktu nebo inhalaci.
Použití
-Roztoky hydrogenuhličitanu vápenatého byly po dlouhou dobu používány k praní starých papírů, zejména uměleckých děl nebo historicky důležitých dokumentů.
-Použití roztoků hydrogenuhličitanu je užitečné nejen proto, že neutralizují kyseliny v papíru, ale také poskytují alkalickou rezervu uhličitanu vápenatého. Tato poslední sloučenina poskytuje ochranu pro budoucí poškození na papíře.
-Jako jiné bikarbonáty se používá v chemických kvasnicích a ve formulacích šumivých tablet nebo prášků. Kromě toho se jako potravinářská přísada používá vodný hydrogenuhličitan vápenatý (vodné roztoky této soli)..
-Roztoky hydrogenuhličitanu se používají při prevenci osteoporózy. V jednom případě však byly pozorovány sekundární účinky jako hyperkalcémie, metabolická alkalóza a selhání ledvin..
-Hydrogenuhličitan vápenatý se příležitostně podává intravenózně, aby se korigoval depresivní účinek hypokalémie na srdeční funkci.
-A konečně, poskytuje tělu vápník, který je prostředníkem svalové kontrakce, a zároveň koriguje acidózu, která se může objevit v hypokalemickém stavu..
Odkazy
- Wikipedia. (2018). Hydrogenuhličitan vápenatý. Převzato z: en.wikipedia.org
- Sirah Dubois. (3. října 2017). Co je hydrogenuhličitan vápenatý? Zdroj: livestrong.com
- Science Learning Hub. (2018). Uhličitanová chemie. Zdroj: sciencelearn.org.nz
- PubChem. (2018). Hydrogenuhličitan vápenatý. Zdroj: pubchem.ncbi.nlm.nih.gov
- Amy E. Gerbracht & Irene Brückleová. (1997). Využití roztoků hydrogenuhličitanu vápenatého a hydrogenuhličitanu hořečnatého v malých dílnách: Výsledky průzkumu. Zdroj: cool.conservation-us.org


