Formulace octanu sodného, příprava, vlastnosti, rizika a použití
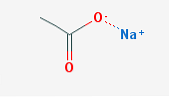
octan sodný, také známý jako ethanoát sodný (zkráceně NaOAc), je sodná sůl kyseliny octové. Jeho chemický vzorec je CH3COONa a má iontovou vazbu mezi sodíkovým iontem a acetátovým iontem.
Tato chemická sloučenina je přirozeně přítomna v rostlinných a živočišných tkáních. Lze jej nalézt v jakékoliv formě, bezvodé nebo trihydrátované. Oba ionty, Na + a CH3COO- jsou přítomny v organismech a plní vitální funkce: sodíkový ion jako regulátor celkové tělesné vody a acetátový ion jako akceptor vodíku (Formulace octanu sodného, 2005-2017).
Index
- 1 Příprava
- 2 Fyzikální a chemické vlastnosti
- 3 Reaktivita a nebezpečí
- 4 Manipulace a skladování
- 5 Použití a aplikace
- 6 Odkazy
Příprava
Octan sodný je sloučenina, která může být připravena jednoduchým a přístupným způsobem pro každého. Obvykle je jeho příprava známa jako "experiment s horkým ledem", protože krystalizace připomíná vodu v pevném stavu (vědec, 2016).
Pro přípravu octanu sodného potřebujete pouze ocet (kyselinu octovou) a uhličitan sodný nebo hydrogenuhličitan sodný. Jednoduše přidejte hydrogenuhličitan do octa, čímž vzniká šumivá reakce, protože podle reakcí uvolňuje oxid uhličitý.
CH3COOH + NaHC033 → CH3COONa + H2CO3
H2CO3 → CO2 + H2O
Uhličitan nebo hydrogenuhličitan sodný mohou být substituovány hydroxidem sodným (louhem), kde se podle reakce vytváří octan sodný a voda:
CH3COOH + NaOH → CH3COONa + H2O
Tato reakce nezpůsobuje šumění, avšak má tu nevýhodu, že s hydroxidem sodným je obtížnější manipulovat než s hydrogenuhličitanem.
Pro dosažení účinku krystalizace (nebo účinku horkého ledu) musí být roztok přesycen zahřátím, aby se hydrogenuhličitan rozpustil v přebytku. Uzavřená nádoba se potom ochladí a potom rekrystalizuje. Následně se krystaly odfiltrují a rozmělní na prášek (degroof, S.F.)..
Fyzikální a chemické vlastnosti
Octan sodný je bílé hygroskopické sklo s octovým zápachem.

V případě bezvodé formy sloučeniny má molekulová hmotnost 82,03 g / mol a hustota je 1,5 g / ml. Jeho bod tání je 324 ° C a jeho bod varu je 881,4 ° C.
Ve své trihydrované formě má molekulovou hmotnost 136,03 g / mol a hustotu 1,45 g / ml. Teplota tání a teploty varu klesají drasticky na 58 ° C a 122 ° C.
Octan sodný je velmi rozpustný ve vodě. Rozpustnost trihydrátu je 46,5 g octanu sodného ve 100 ml vody při teplotě 20 stupňů Celsia, a ve své bezvodé formě může rozpustit 123 g na 100 ml vody (Národní centrum pro biotechnologické informace, 2017 ).
Obě formy jsou rozpustné v acetonu, methanolu, hydrazinu a trihydrátová forma je rozpustná v ethanolu. Octan sodný má monoklinickou krystalickou strukturu (Royal Society of Chemistry, 2015).
Octan sodný je konjugovaná báze kyseliny octové, takže můžete použít roztok kyseliny octové / octanu sodného k přípravě roztoků pufru, aby bylo možné kontrolovat pH.
Roztok octanu sodného ve vodě je slabě alkalický. Když je teplo vyšší než 324 stupňů Celsia, tato sůl se rozkládá a vytváří výpary kyseliny octové.
Reaktivita a nebezpečí
Octan sodný je klasifikován jako stabilní sloučenina a nekompatibilní s oxidačními činidly. Při zahřívání se mohou vytvářet páry kyseliny octové a uvolňování CO2. Sloučenina může být hořlavá při vysokých teplotách uvolňujících CO a CO2.
Bezpečnost octanu sodného byla rozsáhle studována na zvířecích modelech potkanů a myší. Při perorálním podání je letální dávka, která zabije polovinu populace krys, 3530 mg octanu sodného na kg tělesné hmotnosti krysy..
Při inhalaci namísto požití je dávka potřebná k usmrcení poloviny populace krysy mnohem vyšší, více než 30 g / m3 za hodinu..
U myší subkutánní nebo subkutánní injekce 3200 mg / kg tělesné hmotnosti zabije polovinu populace myší, podobnou požití octanu sodného u potkanů..
Nicméně u myší, když jsou podávány orálně, mohou snášet mnohem více než krysy; je smrtelná dávka pro polovinu populace myší 6891 mg / kg tělesné hmotnosti.
U lidí může inhalace octanu sodného způsobit kašel a bolest v krku, zatímco přímý kontakt kůže nebo očí může způsobit zarudnutí a podráždění. Obecně však toxicita u lidí je minimální (WASSERMAN, 2015).
To může způsobit podráždění zažívacího ústrojí s bolestí břicha, nevolnost, zvracení a ovlivnit močový systém. Vdechnutí sloučeniny může způsobit podráždění dýchacích cest. Symptomy mohou zahrnovat kašel, bolest v krku, dušnost a bolest na hrudi.
V případě kontaktu s očima je třeba kontaktní čočky zkontrolovat a odstranit. Oči by měly být okamžitě omyty velkým množstvím vody po dobu nejméně 15 minut. Můžete použít studenou vodu. Pokud dojde k podráždění, je třeba zajistit lékařskou pomoc.
V případě kontaktu s pokožkou je třeba ji omýt vodou a mýdlem. Můžete použít studenou vodu. Podrážděná pokožka je pokryta změkčovadlem. Pokud dojde k podráždění očí, je třeba, stejně jako při očním kontaktu, zajistit lékařskou pomoc.
Pokud se vdechne, oběť by měla být přemístěna na chladné místo. Pokud nedýchá, má se podat umělé dýchání. Pokud je dýchání obtížné, musí být zajištěn kyslík. Znovu je nutné okamžitě vyhledat lékařskou pomoc.
V případě požití by nemělo být vyvoláno zvracení, pokud to výslovně neuvádí zdravotnický personál. Osobě v bezvědomí nikdy nedávejte nic ústy.
Volný oděv, například límec na košili, kravatu nebo pásek, by měl být uvolněn. Pokud se objeví příznaky, je třeba zajistit lékařskou pomoc (Bezpečnostní list materiálu bezvodý octan sodný, 2013).
Manipulace a skladování
-Sloučenina by měla být udržována mimo dosah tepla a zdrojů vznícení
-Prázdné nádoby představují nebezpečí požáru, zbytek vypařte pod odsavačem
-Elektrické zařízení musí být uzemněno, aby nedošlo k jiskření
-Nepolykejte ani nevdechujte prach
-Používejte vhodný ochranný oděv
-V případě nedostatečné ventilace je třeba použít odpovídající dýchací přístroj
-V případě požití okamžitě vyhledejte lékaře a ukažte obal nebo označení
-Činidlo by nemělo být uchováváno v blízkosti neslučitelných látek, jako jsou oxidační činidla a kyseliny.
-Uchovávejte obal těsně uzavřený, kromě toho, aby byl obal uchováván na chladném a dobře větraném místě.
Použití a aplikace
Octan sodný se používá v extrémně rozmanitých průmyslových odvětvích. V textilním průmyslu acetát sodný neutralizuje odpadní proudy kyseliny sírové a také jako fotorezist při použití anilinových barviv. To zlepšuje kvalitu hotových tkanin.
Na fotografii je octan sodný součástí roztoku vývojky a působí jako fotorezist. Octan sodný se používá ke zmírnění škod způsobených vodou na beton tím, že působí jako tmel, přičemž je šetrný k životnímu prostředí a levnější než běžně používaná alternativa epoxidu k utěsnění betonu proti pronikání vody..
Je také mořícím činidlem při opalování chromu a pomáhá zabránit vulkanizaci chloroprenu při výrobě syntetického kaučuku. Při zpracování bavlny pro jednorázové vatové tampóny se používá acetát sodný, který eliminuje tvorbu statické elektřiny.
Octan sodný přidávaný do potravin působí jako konzervační činidlo a ochucovadlo. Zejména bramborové lupínky s octanem sodným mají výraznou chuť "soli a octa".
Octan sodný se také používá v topných polštářích, ohřívačích rukou a horkém ledu. Krystaly trihydrátu octanu sodného se roztaví při 58,4 ° C a rozpustí se v jejich krystalizační vodě.
Po zahřátí nad teplotu tání a následném ochlazení se vodný roztok přesycí. Tento roztok se může ochladit na teplotu místnosti bez tvorby krystalů.
Stisknutím kovového disku do zahřívací podložky se vytvoří nukleační centrum, které způsobí, že roztok krystalizuje zpět do pevného trihydrátu octanu sodného. Proces tvorby krystalů je exotermní. Latentní teplo fúze je přibližně 264-289 kJ / kg.
Na rozdíl od některých typů tepelných balení, jako jsou závislé nevratné chemické reakce, je tepelná jednotka octanu sodného může být snadno znovu ponořením balíček ve vroucí vodě po dobu několika minut, dokud se krystaly nerozpustí a umožňuje že balení pomalu vychladne, dokud nedosáhne pokojové teploty.
Roztoky octanu sodného a kyseliny octové působí jako pufry pro udržení relativně konstantního pH, což je užitečná vlastnost jak pro biochemické výzkumné reakce, tak pro ropný průmysl a kosmetický průmysl..
Octan sodný může být použit pro precipitaci malých nukleových kyselin. Tato precipitace může být použita pro koncentraci malých nukleových kyselin ze zředěných roztoků, jako je například pufr s nižší funkcí po frakcionaci flashPAGE.
Když je do mlecího zařízení flashPAGE vloženo méně než 2 μg nukleové kyseliny, doporučuje se srážení s octanem sodným / ethanolem přes noc s vehikulem, jako je lineární akrylamid nebo glykogen, pro maximální regeneraci nukleové kyseliny z běžícího pufru. pomalý.
Použití glykogenu jako nosiče se nedoporučuje pro vzorky, které budou použity pro analýzu DNA čipů (precipitace sodné soli kyseliny octové malých nukleových kyselin, S.F.)..
V oblasti medicíny léčí roztoky octanu sodného pacienty s vysokými hladinami krevních kyselin a / nebo nízkými hladinami sodíku.
Sodík je hlavním kationtem extracelulární tekutiny. Obsahuje více než 90% celkových kationtů při normální plazmatické koncentraci přibližně 140 mEq / litr. Sodný iont hraje klíčovou roli v kontrole celkové tělesné vody a její distribuci (Acetát sodný, 2010).
Acetát je akceptor vodíkových iontů. Slouží také jako alternativní zdroj hydrogenuhličitanu (HCO3-) pro metabolickou přeměnu v játrech. Bylo prokázáno, že tato konverze probíhá snadno, a to i za přítomnosti závažného onemocnění jater.
Injekce octanu sodného zředěného vodou se podává intravenózně jako doplněk elektrolytu. Každý 20 ml obsahuje 3,28 g octanu sodného, který obsahuje 40 mEq sodíku (Na +) a acetátu (HCO).3-). Roztok neobsahuje bakteriostat, antimikrobiální činidlo ani přidaný pufr. Může obsahovat kyselinu octovou pro úpravu pH (pH je 6,5 (6,0 až 7,0)). Osmolová koncentrace je 4 mOsmol / ml (calc).
Řešení je považováno za alternativu k chloridu sodnému za účelem získání sodíkových iontů (Na +) pro jeho přidání do vysoce objemných infuzních tekutin pro intravenózní použití (Acetát sodný, 2009).
Roztoky obsahující ionty sodíku by měly být používány s velkou opatrností, zejména v případech pacientů s městnavým srdečním selháním, těžkým selháním ledvin a v klinických stavech, při kterých dochází k edému s retencí sodíku..
U pacientů s poruchou funkce ledvin může podání roztoků obsahujících ionty sodíku vést k retenci sodíku. Roztoky obsahující acetátové ionty by měly být používány s velkou opatrností u pacientů s metabolickou nebo respirační alkalózou.
Acetát musí být podáván s velkou opatrností v těch stavech, ve kterých dochází ke zvýšení hladiny nebo zhoršenému užívání tohoto iontu, jako je těžká jaterní insuficience..
Odkazy
- (S.F.). Jak si vyrobit acetát sodný z domácích surovin. Recuperado de instructables: instructables.com.
- Bezpečnostní list materiálu Bezvodý octan sodný. (2013, 21. května). Získané z sciencelab: sciencelab.com.
- Národní centrum pro biotechnologické informace. (2017, 4. března). PubChem Compound Database; CID = 517045. Získáno z PubChem.
- Královská chemická společnost. (2015). Octan sodný. Zdroj: chemspider.com.
- vědec, D. N.-c. (2016, 12. srpna). "HOT ICE" - úžasný experiment. Zdroj: youtube.com.
- Acetát sodný. (2009, 19. května). Získáno z rxlistu.
- Acetát sodný. (2010, duben). Získané z drug.com.
- Formulace octanu sodného. (2005–2017). Obnoveno z softschools.com.
- Srážení sodných acetátů malých nukleových kyselin. (S.F.). Znovuzískané z termofisheru.
- WASSERMAN, R. (2015, 16. srpna). Co je sodná sůl kyseliny octové? Zdroj: livestrong: livestrong.com.


