Vlastnosti, typy a funkce mikroskopů
mikrosomy jsou to fragmenty membrán, které tvoří malé a uzavřené váčky. Tyto struktury vznikají reorganizací uvedených fragmentů, obvykle pocházejí z endoplazmatického retikula po buněčné homogenizaci. Vezikuly mohou být kombinací membrán zprava z vnějšku, zevnitř do vnějšku nebo tavené.
Všimněte si, že mikrosomy jsou artefakty, které se objevují díky procesu buněčné homogenizace, vytvářejí rozmanité a komplexní umělé struktury. Teoreticky se mikrosomy nevyskytují jako normální prvky živých buněk.
 Vnitřek mikrosomu je variabilní. V lipidové struktuře mohou být různé proteiny, které nejsou navzájem příbuzné. Mohou mít také proteiny připojené k vnějšímu povrchu.
Vnitřek mikrosomu je variabilní. V lipidové struktuře mohou být různé proteiny, které nejsou navzájem příbuzné. Mohou mít také proteiny připojené k vnějšímu povrchu.
V literatuře, termín “jaterní mikrosom” vyniká, který se odkazuje na struktury tvořené jaterními buňkami, zodpovědný za důležité metabolické transformace příbuzné enzymatickému aparátu endoplasmic reticulum \ t.
Jaterní mikrosomy byly již dlouho experimenty in vitro farmaceutického průmyslu. Tyto malé vezikuly jsou adekvátní strukturou pro provádění experimentů metabolismu léčiv, protože obsahují enzymy zapojené do procesu, včetně CYP a UGT..
Index
- 1 Historie
- 2 Charakteristiky
- 2.1 Složení
- 2.2 Sedimentace při odstředění
- 3 Typy
- 4 Funkce
- 4.1 V buňce
- 4.2 Ve farmaceutickém průmyslu
- 5 Odkazy
Historie
Mikrosomy byly pozorovány po dlouhou dobu. Termín byl vytvořen vědeckým rodákem Francie jmenoval Claude, když on pozoroval finální produkty centrifugace jaterní hmoty \ t.
V polovině 60. let výzkumník Siekevitz spojil mikrosomy se zbytky endoplazmatického retikula po provedení procesu homogenizace buněk.
Vlastnosti
V buněčné biologii je mikrosomem vezikula tvořená membránami z endoplazmatického retikula.
Během rutinních buněčných ošetření prováděných v laboratoři praskly eukaryotické buňky a přebytečné membrány se opět seskupily ve formě vezikul, což vedlo k vzniku mikrosomů..
Velikost těchto vezikulárních nebo tubulárních struktur je v rozmezí 50 až 300 nanometrů.
Mikrosomy jsou laboratorní artefakty. Proto v živé buňce a za normálních fyziologických podmínek tyto struktury nenajdeme. Jiní autoři, na druhé straně, ujistit se, že oni nejsou artefakty, a že oni jsou skutečné organelles přítomné v intaktních buňkách (vidět více v Davidson a Adams, 1980) \ t
Složení
Složení membrány
Strukturálně jsou mikrosomy identické s membránou endoplazmatického retikula. V buněčném interiéru je síť membrán retikula tak rozsáhlá, že tvoří více než polovinu všech membrán buněk..
Mřížka je tvořena řadou trubiček a sáčků nazývaných cisterny, obě jsou tvořeny membránami.
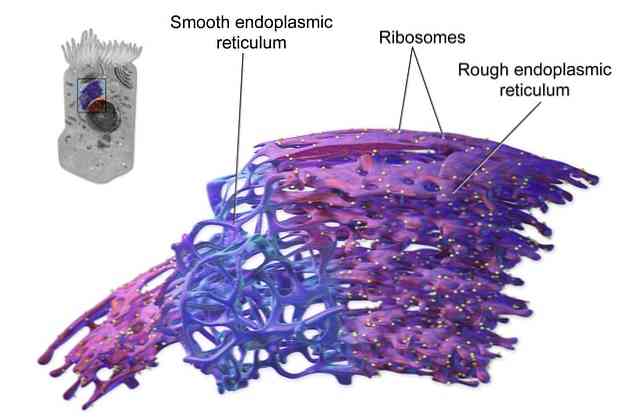
Tento membránový systém tvoří spojitou strukturu s membránou buněčného jádra. Dva typy mohou být diferencovány v závislosti na přítomnosti nebo ne na ribozomech: hladké a hrubé endoplazmatické retikulum. Pokud jsou mikrosomy ošetřeny určitými enzymy, mohou být uvolněny ribozomy.
Vnitřní složení
Mikrosomy jsou bohaté na různé enzymy, které se obvykle nacházejí uvnitř endoplazmatického hladkého jaterního retikula.
Jedním z nich je enzym cytochrom P450 (zkratka CYP, zkratka v angličtině). Tento katalytický protein používá jako substráty širokou řadu molekul.
CYP jsou součástí řetězce přenosu elektronů a jeho nejčastější reakce se nazývají monooxygenáza, kde do substrátu organické povahy vloží atom kyslíku a zbývající atom kyslíku (používá molekulární kyslík, O2) se sníží na vody.
Mikrosomy jsou také bohaté na jiné membránové proteiny, jako je UGT (uridinadifosfát glukuronyltransferáza) a FMO (rodina proteinů monooxygenázy obsahujících flavin). Kromě toho obsahují esterázy, amidázy, epoxidové hydrolázy, mezi jinými proteiny.
Sedimentace při centrifugaci
V laboratořích biologie existuje rutinní technika nazývaná centrifugace. V tomto je možné oddělit pevné látky s použitím jako diskriminační vlastnosti různé hustoty složek směsi.
Když jsou buňky odstředěny, oddělují se různé složky a sraženina (to znamená, že jdou dolů na dno zkumavky) v různých časech a při různých rychlostech. Jedná se o metodu, která se použije, když chcete vyčistit určitou specifickou buněčnou složku.
Když odstřeďují neporušené buňky, první věc k sedimentu nebo sraženina jsou těžší elementy: jádra a mitochondria. K tomu dochází při méně než 10 000 gravitacích (rychlost v odstředivkách je kvantifikována v gravitacích). Mikroskopy sedimentují, když jsou aplikovány mnohem vyšší rychlosti, řádově 100 000 gravitací.
Typy
Termín mikrosom se v současné době používá v širokém smyslu k označení jakéhokoliv vezikulu vytvořeného díky přítomnosti membrán, buď mitochondrií, Golgiho aparátu nebo buněčné membrány jako takové..
Vědci však nejvíce používají mikrosomy jater, díky enzymatickému složení interiéru. Z tohoto důvodu jsou v literatuře nejvíce zmiňovanými typy mikrosomů.
Funkce
V cele
Jako mikrosomy jsou a artefakt vytvořené procesem buněčné homogenizace, to znamená, že nejsou prvky, které běžně nacházíme v buňce, nemají asociovanou funkci. Nicméně, oni mají důležité aplikace ve farmaceutickém průmyslu.
Ve farmaceutickém průmyslu
Ve farmaceutickém průmyslu jsou mikrosomy široce používány při objevování léčiv. Mikrosomy umožňují prostým způsobem studovat metabolismus sloučenin, které chce výzkumník hodnotit.
Tyto umělé váčky mohou být zakoupeny z mnoha biotechnologických továren, které je získávají pomocí diferenciální centrifugace. Během tohoto procesu se na buněčný homogenát aplikují různé rychlosti, což vede k získání čištěných mikrosomů.
Enzymy cytochromu P450, které se nacházejí v mikrosomech, jsou zodpovědné za první fázi metabolismu xenobiotik. Jedná se o látky, které se přirozeně nevyskytují v živých bytostech a neočekávali bychom je přirozeně. Obecně musí být metabolizovány, protože většina z nich je toxická.
Jiné proteiny, které jsou také umístěny uvnitř mikrosomu, jako je rodina proteinů monooxygenázy, které obsahují flavin, jsou také zapojeny do oxidačního procesu xenobiotik a usnadňují jejich vylučování..
Mikrosomy jsou tedy dokonalými biologickými entitami, které umožňují vyhodnotit reakci organismu na určité léky a léky, protože mají enzymatické mechanismy nezbytné pro metabolismus uvedených exogenních sloučenin..
Odkazy
- Davidson, J., & Adams, R. L. P. (1980). Biochemie nukleových kyselin Davidson .Obrátil jsem se.
- Faqi, A. S. (Ed.). (2012). Komplexní průvodce toxikologií v předklinickém vývoji léčiv. Akademická tisková zpráva.
- Fernández, P. L. (2015). Velázquez Základní a klinická farmakologie (online eBook). Panamericana Medical.
- Lam, J.L., & Benet, L. Z. (2004). Studie jaterních mikrosomů nejsou dostatečné k charakterizaci in vivo metabolismu v játrech a metabolických lékových interakcí: studie metabolismu digoxinu u primárních hepatocytů potkana versus mikrosomy. Metabolismus a dispozice léčiv, 32(11), 1311-1316.
- Palade, G.E., & Siekevitz, P. (1956). Jaterní mikrozomy; integrovaná morfologická a biochemická studie. Žurnál biofyzikální a biochemické cytologie, 2(2), 171-200.
- Stillwell, W. (2016). Úvod do biologických membrán. Newnes.
- Taylor, J. B., & Triggle, D. J. (2007). Komplexní medicinální chemie II. Elsevier.


