Vlastnosti jodoátu draselného, struktura, použití a rizika
jodičnan draselný nebo jodičnan draselný je anorganická sloučenina jodu, konkrétně sůl, jejíž chemický vzorec je KIO3. Jod, prvek skupiny halogenů (F, Cl, Br, I, As), má v této soli oxidační číslo +5; proto je to silné oxidační činidlo. KIO3 disociuje ve vodném médiu za vzniku iontů K+ a IO3-.
Je syntetizován reakcí hydroxidu draselného s kyselinou jodovou: HIO3(aq) + KOH (s) => KIO3(aq) + H2O (l) Také může být syntetizován reakcí molekulárního jodu s hydroxidem draselným: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

Index
- 1 Fyzikální a chemické vlastnosti
- 1.1 Oxidační činidlo
- 2 Chemická struktura
- 3 Použití a aplikace jodičnanu draselného
- 3.1 Terapeutické použití
- 3.2 Použití v průmyslu
- 3.3 Analytické použití
- 3.4 Použití v technologii laserů
- 4 Zdravotní rizika jodičnanu draselného
- 5 Odkazy
Fyzikální a chemické vlastnosti
Je to bílá pevná látka bez zápachu, s jemnými krystaly a krystalickou strukturou monoklinického typu. Má hustotu 3,98 g / ml, molekulovou hmotnost 214 g / mol a má absorpční pásy v infračerveném (IR) spektru.
Má bod tání: 833 ºK (560 ºC), což odpovídá silným iontovým interakcím mezi ionty K+ a IO3-. Při vyšších teplotách se podrobuje tepelné rozkladné reakci, která uvolňuje molekulární kyslík a jodid draselný:
2KIO3(s) => 2KI (s) + 3O2(g)
Ve vodě má rozpustnosti, které se pohybují od 4,74 g / 100 ml do 0 ° C, až do 32,3 g / 100 ml při 100 ° C, čímž vznikají bezbarvé vodné roztoky. Kromě toho je nerozpustný v alkoholu a kyselině dusičné, ale je rozpustný ve zředěné kyselině sírové.
Jeho afinita k vodě není znatelná, což vysvětluje, proč není hygroskopická a neexistuje ve formě hydratovaných solí (KIO)3H2O).
Oxidační činidlo
Jodičnan draselný, jak naznačuje chemický vzorec, má tři atomy kyslíku. Toto je silně electronegative element a, kvůli této vlastnosti, to “odhalí” elektronický nedostatek v oblaku obklopovat jód \ t.
Tento nedostatek - případně příspěvek - může být vypočítán jako oxidační číslo jodu (± 1, +2, +3, +5, +7), které je +5 pro případ této soli..
Co to znamená? Že před druhem schopným dávat jeho elektrony, jód přijme je v jejich iontové formě (IO3-), aby se stal molekulárním jodem a měl oxidační číslo rovné 0.
Po tomto vysvětlení může být stanoveno, že jodičnan draselný je oxidační sloučenina, která silně reaguje s redukčními činidly v mnoha redox reakcích; ze všech těchto je jeden známý jako jódové hodiny.
Jódové hodiny se skládají z redoxního procesu pomalých a rychlých kroků, ve kterém jsou rychlé kroky označeny řešením KIO3 v kyselině sírové, ke které se přidá škrob. Dále, škrob - kdysi vyrobený a ukotvený mezi jeho strukturou druhu I3-- roztok změní barvu z bezbarvé na tmavě modrou.
IO3- + 3 HSO3- → I- + 3 HSO4-
IO3- + 5 I- + 6 H+ → 3 I2 + 3H2O
Já2 + HSO3- + H2O → 2 I- + HSO4- + 2 H+ (tmavě modrá v důsledku škrobového účinku)
Chemická struktura
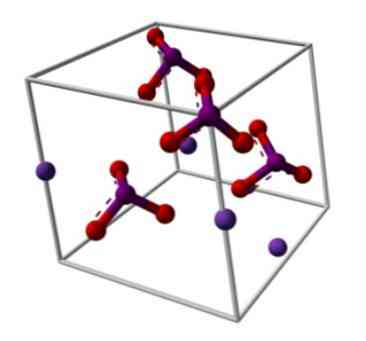
Chemická struktura jodičnanu draselného je znázorněna na horním obrázku. IO anion3- je reprezentován “stativem” červené a purpurové koule, zatímco K ionty+ jsou reprezentovány fialovými kuličkami.
Co ale tyto stativy znamenají? Správné geometrické tvary těchto anionů jsou vlastně trigonální pyramidy, ve kterých kyslíky tvoří trojúhelníkovou základnu, a nesdílený pár elektronů v jódových bodech vzhůru, zabírající prostor a nutící spojení IO dolů a dva odkazy I = O.
Tato molekulární geometrie odpovídá sp hybridizaci3 centrálního atomu jodu; nicméně, jiný pohled navrhne, že jeden z atomů kyslíku tvoří vazby s “d” orbitals jodu, být ve skutečnosti sp hybridizace3d2 (jód může mít jeho “d” orbitals rozšiřovat jeho valence shell) \ t.
Krystaly této soli mohou projít přechodem strukturní fáze (jiné uspořádání než monoklinické) v důsledku různých fyzikálních podmínek, které je vystavují.
Použití a aplikace jodičnanu draselného
Terapeutické použití
Jodičnan draselný se obvykle používá k zabránění hromadění radioaktivity ve štítné žláze ve formě 131I, když se tento izotop používá při stanovení příjmu jódu štítnou žlázou jako součást funkce štítné žlázy.
Podobně se jodičnan draselný používá jako lokální antiseptikum (0,5%) při slizničních infekcích.
Použití v průmyslu
Přidává se do krmiva hospodářských zvířat jako doplněk jodu. Proto se v průmyslu používá jodičnan draselný ke zlepšení kvality mouky.
Analytické použití
V analytické chemii se díky své stabilitě používá jako primární standard při standardizaci standardních roztoků thiosíranu sodného (Na \ t2S2O3), aby se stanovily koncentrace jodu ve vzorcích.
To znamená, že množství jodu může být známo volumetrickou technikou (titrací). V této reakci jodičnan draselný rychle oxiduje jodidové ionty I-, následující chemickou rovnicí:
IO3- + 5I- + 6H+ => 3I2 + 3H2O
Jód, já2, je pojmenován roztokem Na2S2O3 pro jeho standardizaci.
Použití v laserové technologii
Studie prokázaly a potvrdily zajímavé piezoelektrické, pyroelektrické, elektrooptické, feroelektrické vlastnosti a v nelineární optice KIO krystalů3. Výsledkem je velký potenciál v oblasti elektroniky a technologie laserů pro materiály vyrobené s touto sloučeninou.
Zdravotní rizika jodičnanu draselného
Ve vysokých dávkách může způsobit podráždění ústní sliznice, kůže, očí a dýchacích cest.
Experimenty toxicity jodičnanu draselného u zvířat umožnily pozorovat, že u psů nalačno, při dávkách 0,2-0,25 g / kg tělesné hmotnosti, podávaných orálně, sloučenina způsobuje zvracení..
Pokud se těmto zvracením vyhnete, způsobí zhoršení situace u zvířat, protože před smrtí vyvolává anorexii a prostraci. Jeho pitvy umožnily pozorovat nekrotické léze v játrech, ledvinách a střevní sliznici.
Vzhledem ke své oxidační síle představuje riziko požáru při styku s hořlavými materiály.
Odkazy
- Den, R., & Underwood, A. Kvantitativní analytická chemie (páté vydání). PEARSON Prentice Hall, p-364.
- Muth, D. (2008). Lasery [Obrázek]. Zdroj: flickr.com
- ChemicalBook. (2017). Jodičnan draselný. Citováno dne 25. března 2018, z ChemicalBook: chemicalbook.com
- PubChem. (2018). Jodičnan draselný. Získal 25. března 2018, od PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Jodičnan draselný. Získáno 25. března 2018 od společnosti Merck:
- merckmillipore.com
- Wikipedia. (2017). Jodičnan draselný. Citováno dne 25. března 2018, z Wikipedie: en.wikipedia.org
- M M Abdel Kader et al. (2013). Mechanismus přenosu náboje a fázové přechody nízkých teplot v KIO3. J. Phys., Conf. Ser. 423 012036


