Oxid vápenatý (CaO) Struktura, vlastnosti a použití
oxid vápenatý (CaO) je anorganická sloučenina, která obsahuje vápník a kyslík v iontových formách (nesmí být zaměňována s peroxidem vápníku, CaO2). To je znáno celosvětově jako vápno, slovo, které označuje nějakou anorganickou sloučeninu, která obsahuje uhličitany, oxidy vápníku a hydroxidy, stejně jako jiné kovy takový jako křemík, hliník a železo..
Tento oxid (nebo vápno) je také označován hovorově jako pálené vápno nebo hasené vápno v závislosti na tom, zda je nebo není hydratován. Vápno je oxid vápenatý, zatímco hasené vápno je jeho hydroxid. Na oplátku, vápenec (vápenec nebo kalené vápno) je vlastně sedimentární hornina složená hlavně uhličitan vápenatý (CaCO3).

Je to jeden z největších přírodních zdrojů vápníku a představuje surovinu pro výrobu oxidu vápenatého. Jak se tento oxid vyrábí? Uhličitany jsou citlivé na tepelný rozklad; zahřívání uhličitanů vápenatých při teplotách nad 825 ° C, což vede k tvorbě vápna a oxidu uhličitého.
Výše uvedené tvrzení lze popsat následovně: CaCO3(s) → CaO (s) + CO2(g) Protože zemská kůra je bohatá na vápenec a kalcit a v oceánech a plážích jsou hojné mořské mušle (suroviny pro výrobu oxidu vápenatého), oxid vápenatý je relativně levné činidlo.
Index
- 1 Vzorec
- 2 Struktura
- 3 Vlastnosti
- 3.1 Rozpustnost
- 4 Použití
- 4.1 Jako malta
- 4.2 Při výrobě brýlí
- 4.3 V hornictví
- 4.4 Jako odstraňovač silikátu
- 5 Nanočástice oxidu vápenatého
- 6 Odkazy
Vzorec
Chemický vzorec oxidu vápenatého je CaO, ve kterém je vápník podobný kyselému iontu (akceptor elektronu) Ca2+, a kyslík jako bazický iont (donor elektronů) OR2--.
Proč má vápník +2 náboj? Protože vápník patří do skupiny 2 periodické tabulky (Mr. Becambara), a má pouze dva valenční elektrony, které jsou k dispozici pro tvorbu vazeb, které se dostávají k atomu kyslíku..
Struktura
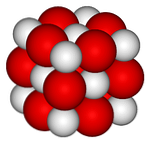
V horním obrázku je znázorněna krystalická struktura (typ gem-soli) pro oxid vápenatý. Objemné červené koule odpovídají iontům Ca2+ a bílé kuličky k iontům O2-.
V tomto uspořádání krychlových krystalů každý iont Ca2+ je obklopen šesti ionty O2-, uzavřené v oktaedrických dírách, které mezi nimi zanechaly velké ionty.
Tato struktura vyjadřuje maximálně iontový charakter tohoto oxidu, ačkoli pozoruhodný rozdíl poloměrů (červená koule je větší než bílá) uděluje slabší krystalickou retikulární energii ve srovnání s MgO..
Vlastnosti
Fyzicky se jedná o krystalickou bílou pevnou látku bez zápachu se silnými elektrostatickými interakcemi, které jsou zodpovědné za její vysoké teploty tání (2572 ° C) a var (2850 ° C). Navíc má molekulovou hmotnost 55,958 g / mol a zajímavou vlastnost je termoluminiscenční.
To znamená, že kus oxidu vápenatého, který je vystaven plameni, může svítit intenzivním bílým světlem, které je známo v angličtině s názvem reflektor, nebo ve španělštině, světlo vápníku. Ca ionty2+, při kontaktu s ohněm způsobují načervenalý plamen, jak ukazuje následující obrázek.

Rozpustnost
CaO je bazický oxid, který má silnou afinitu k vodě, do té míry, že absorbuje vlhkost (jedná se o hygroskopickou pevnou látku), která okamžitě reaguje za vzniku haseného vápna nebo hydroxidu vápenatého:
CaO (s) + H2O (l) => Ca (OH)2(s)
Tato reakce je exotermní (uvolňuje teplo) v důsledku tvorby pevné látky se silnějšími interakcemi a stabilnější krystalové mřížky. Reakce je však reverzibilní, pokud se Ca (OH) zahřívá2, dehydrataci a rozsvícení hašeného vápna; pak vápno "znovuzrozené".
Výsledný roztok je velmi bazický a pokud je nasycen oxidem vápenatým, dosahuje pH 12,8.
Podobně je rozpustný v glycerolu a v roztocích kyseliny a cukru. Jelikož se jedná o bazický oxid, má přirozeně účinné interakce s oxidy kyselin (SiO)2, Al2O3 a víra2O3, například rozpustné v kapalných fázích. Na druhé straně je nerozpustný v alkoholech a organických rozpouštědlech.
Použití
CaO má obrovské množství průmyslových použití, stejně jako v syntéze acetylenu (CH≡CH), při extrakci fosfátů z odpadních vod a při reakci s oxidem siřičitým z plynného odpadu..
Další použití oxidu vápenatého jsou popsána níže:
Jako malta
Pokud se oxid vápenatý smísí s pískem (SiO)2) a vody, koláče s pískem a pomalu reaguje s vodou za vzniku haseného vápna. Na druhé straně, CO2 vzduchu se rozpouští ve vodě a reaguje se solí za vzniku uhličitanu vápenatého:
Ca (OH)2(s) + CO2(g) => CaCO3(s) + H2O (l)
CaCO3 Jedná se o odolnější a tvrdší směs než CaO, což způsobuje, že malta (předchozí směs) ztvrdne a fixuje cihly, bloky nebo keramiku mezi nimi nebo na požadovaný povrch..
Při výrobě brýlí
Základní surovinou pro výrobu skel jsou oxidy křemíku, které jsou smíchány s vápnem, uhličitanem sodným (Na2CO3) a dalších přísad, které se potom podrobí ohřevu, což vede ke sklovité pevné látce. Tato pevná látka se následně zahřeje a vyfoukne v libovolných obrázcích.
V hornictví
Hašené vápno zaujímá větší objem než pálené vápno kvůli interakcím s vodíkovými vazbami (O-H-O). Tato vlastnost se používá k rozbití skal zevnitř.
Toho je dosaženo tím, že je naplní kompaktní směsí vápna a vody, která je utěsněna, aby zaměřila své teplo a expanzivní sílu ve skále..
Jako odstraňovač silikátu
CaO se taví s křemičitany za vzniku koalescenční kapaliny, která se pak extrahuje ze suroviny určitého produktu..
Například železné rudy jsou surovinou pro výrobu kovového železa a oceli. Tyto minerály obsahují silikáty, které jsou nežádoucími nečistotami pro proces a jsou eliminovány právě popsanou metodou.
Nanočástice oxidu vápenatého
Oxid vápenatý může být syntetizován jako nanočástice, přičemž se mění koncentrace dusičnanu vápenatého (Ca (NO)3)2) a hydroxid sodný (NaOH) v roztoku.
Tyto částice jsou sférické, základní (stejně tak jako makroskopická pevná látka) a mají velký povrch. V důsledku toho tyto vlastnosti prospívají katalytickým procesům. Co? Vyšetřování v současnosti odpovídá na tuto otázku.
Tyto nanočástice byly použity pro syntézu substituovaných organických sloučenin - odvozených od pyridinů - ve formulaci nových léčiv pro provádění chemických transformací, jako je umělá fotosyntéza, pro čištění vody z těžkých a škodlivých kovů a jako fotokatalytických činidel.
Nanočástice mohou být syntetizovány na biologickém nosiči, jako jsou listy papáji a zeleného čaje, které mohou být použity jako antibakteriální činidlo..
Odkazy
- scifun.org (2018). Vápno: oxid vápenatý. Získáno 30. března 2018, z: scifun.org.
- Wikipedia. (2018). Oxid vápenatý. Získáno 30. března 2018, z: en.wikipedia.org
- Ashwini Anantharaman a kol. (2016). Zelená syntéza nanočástic oxidu vápenatého a jeho aplikace. Int. Journal of Engineering Research and Application. ISSN: 2248-9622, svazek 6, vydání 10, (část -1), str. 27-31.
- J. Safaei-Ghomi et al. (2013). Nanočástice oxidu vápenatého katalyzovaly jednokrokovou vícesložkovou syntézu vysoce substituovaných pyridinů ve vodném ethanolovém médiu Scientia Iranica, Transakce C: Chemie a chemické inženýrství 20 549-554.
- PubChem. (2018). Oxid vápenatý. Získáno 30. března 2018, z: pubchem.ncbi.nlm.nih.gov
- Shiver a Atkins. (2008). Anorganická chemie In Prvky skupiny 2. (čtvrté vydání, strana 280). Mc Graw Hill.


