Chemická struktura síranu amonného, vlastnosti a použití
síranu amonného Je to ternární a amonná anorganická sůl kyseliny sírové. Jeho chemický vzorec je (NH4)2SO4. Proto stechiometrické poměry říkají, že pro každý síranový aniont jsou s ním v interakci dva amoniové kationty. To umožňuje neutralitu soli ((+1) ∙ 2 + (-2)).
Její názvosloví je způsobeno skutečností, že se jedná o sůl odvozenou od H2SO4, změna přípony "uric" na "ato". Dva počáteční protony jsou tedy nahrazeny NH4+, reakční produkt s amoniakem (NH.)3). Pak chemická rovnice pro jeho syntézu je: 2 NH3 + H2SO4 => (NH4)2SO4
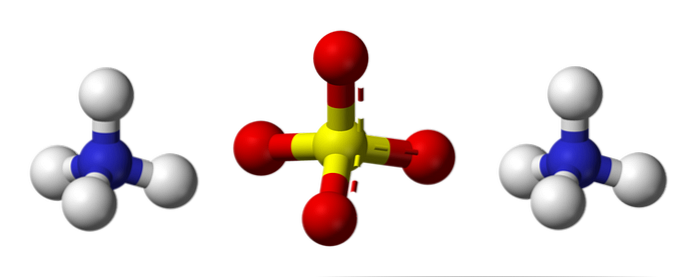
Síran amonný je sklad dusíku a síry, oba nepostradatelné v chemii půd a hnojiv.
Index
- 1 Chemická struktura
- 2 Fyzikální a chemické vlastnosti
- 2.1 Molekulová hmotnost
- 2.2 Fyzický vzhled
- 2.3 Vůně
- 2.4 Bod tání
- 2.5 Rozpustnost
- 2.6 Hustota
- 2.7 Tlak par
- 2.8 Bod vzplanutí
- 2,9 pH
- 2.10 Stabilita
- 2.11 Rozklad
- 2.12 Koroze
- 3 Použití
- 3.1 V zemědělství
- 3.2 Jako analytické činidlo
- 3.3 Při srážení a izolaci proteinů
- 3.4 V průmyslu
- 3.5 Další použití
- 4 Odkazy
Chemická struktura
Horní obrázek znázorňuje molekulární geometrie iontů NH4+ a SO42-. Červené koule odpovídají atomům kyslíku, bílé koule odpovídají atomům vodíku, modré koule atomu dusíku a žluté koule odpovídají atomu síry..
Oba ionty mohou být považovány za dva tetrahedrony, takže mají tři jednotky, které interagují za vzniku ortorombického krystalického uspořádání. Sulfátový anion je SO42- a je schopen darovat nebo přijímat čtyři vodíkové vazby, stejně jako NH kation4+.
Fyzikální a chemické vlastnosti
Molekulová hmotnost
132,134 g / mol.
Fyzický vzhled
Plně bílá. Ortorombické bílé nebo hnědé krystaly, v závislosti na úrovni nečistot.
Vůně
WC.
Teplota tání
280 ° C. Tato teplota tání, nízká ve srovnání s jinými iontovými sloučeninami, je způsobena skutečností, že se jedná o sůl s monovalentními kationty (+1) as odlišnými ionty v jejích velikostech, což způsobuje, že pevná látka má nízkou krystalickou sítnicovou energii.
Rozpustnost
76,4 g / 100 g vody při 25 ° C. Tato afinita k vodě je způsobena velkou kapacitou jejích molekul solvatovat amonné ionty. Na druhé straně je nerozpustný v acetonu a v alkoholu; v rozpouštědlech méně polárních než voda.
Hustota
1,77 g / cm3 při 25 ° C.
Tlak páry
1,871 kPa při 20 ° C.
Bod vznícení
26 ° C.
pH
5,0 - 6,0 (25 ° C, 1 M roztok). Mírně kyselé pH je způsobeno hydrolýzou NH4+ ve vodě, produkující H3O+ při nízkých koncentracích.
Stabilita
Stabilní ve vhodných podmínkách prostředí. Při styku se silnými oxidanty se může vznítit.
Rozklad
Začíná se rozkládat při 150 ° C, uvolňuje toxické páry oxidu siřičitého, oxidů dusíku a amoniaku.
Koroze
Nepoškozuje železo nebo hliník.
Použití

V zemědělství
- Síran amonný se používá jako hnojivo v alkalických půdách. Amonná sůl má ve svém složení 21% dusíku a 24% síry. Existují však sloučeniny, které poskytují větší množství dusíku než síran amonný; Výhodou posledně uvedeného je jeho vysoká koncentrace síry.
- Síra je nezbytná při syntéze proteinů, protože několik aminokyselin, jako je cystin, methionin a cystein, má síru. Z těchto důvodů je síran amonný i nadále jedním z nejdůležitějších hnojiv.
- Používá se v plodinách pšenice, kukuřice, rýže, bavlny, brambor, konopí a ovocných stromů.
- Nízké pH alkalických půd díky jejich podílu na nitrifikačním procesu prováděném mikroby. Používá se amonium (NH)4+) na výrobu dusičnanů (NO3-) a uvolnění H+: 2NH4+ + 4O2 => 2NO3- + 2H2O + 4H+. Zvýšení koncentrace vodíku snižuje pH alkalických půd a umožňuje větší využití.
- Kromě použití jako hnojiva působí síran amonný jako pomocný prostředek pro rozpustné insekticidy, herbicidy a fungicidy, které se nastříkají na plodiny..
- Sulfát je schopen sekvestrovat ionty přítomné v půdě a v zavlažovací vodě, které jsou nezbytné pro život některých patogenů. Mezi ionty, které zachycuje síran amonný, patří Ca2+, Mg2+, víra2+ a víra3+. Tento účinek zvyšuje mikrobicidní účinek uvedených činidel.
Jako analytické činidlo
Síran amonný působí jako precipitační činidlo při elektrochemické analýze, v mikrobiologických kultivačních médiích a při přípravě amonných solí..
Při srážení a izolaci proteinů
Síran amonný se používá při izolaci a čištění proteinů, zejména plazmatických proteinů. Do plazmy se přidá určité množství síranu amonného do určité koncentrace; je tak způsobeno srážení skupiny proteinů.
Sraženina se shromáždí odstředěním a do supernatantu se přidá další množství síranu amonného a při nové koncentraci dojde k vysrážení jiné skupiny proteinů..
Opakování předchozího postupu v sekvenční formě umožňuje získat různé frakce plazmatických proteinů.
Předtím, než se objeví nové technologie molekulární biologie, tento postup umožnil izolovat plazmatické proteiny velkého významu v medicíně, například: imunoglobuliny, koagulační faktory atd..
V průmyslu
Sulfát amonný působí na zpomalení začátku požáru v textilním průmyslu. Používá se jako přísada v elektrolytickém průmyslu. Používá se také při výrobě peroxidu vodíku, chloridu amonného atd..
Ostatní použití
- Síran amonný se používá jako regulační činidlo osmotického tlaku a jako činidlo srážející sůl.
- Ve formě amonium laurylsulfátu klesá povrchové napětí vody, což umožňuje separaci znečišťujících látek zvýšením tvrdosti vody..
- Je to antikorozní prostředek.
- Používá se jako přísada do potravin, která reguluje kyselost v moučném těstě a chlebu.
Odkazy
- OECD SIDS. (Říjen 2004). Síran amonný. [PDF] Získáno 27. dubna 2018, z: inchem.org
- Společnost Mosaic. (2018). Síran amonný. Získáno dne 27. dubna 2018, z: cropnutrition.com
- Wikipedia. (2018). Síran amonný. Získáno dne 27. dubna 2018, z: en.wikipedia.org
- Pubchem. (2018). Síran amonný. Citováno dne 27. dubna 2018, z: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23. července 2015). [Obrázek] Získáno dne 27. dubna 2018, z: flickr.com
- Paula Papp (22. února 2017). Aplikace a použití síranu amonného. Získáno dne 27. dubna 2018, z: business.com


