Saponifikační reakce a látky, které mohou být získány
zmýdelnění Jedná se o základní hydrolýzu esteru. To znamená, že ester reaguje s bází (NaOH nebo KOH) nevratně, čímž vzniká alkohol a karboxyláty sodíku nebo draslíku. Slovo znamená "výrobu mýdel" a ve skutečnosti je jednou z nejstarších chemických reakcí používaných lidstvem.
V babylonských dobách, s pomocí popela získaného ze dřeva a rostlin a živočišných tuků, zdokonalili umění výroby mýdel. Proč živočišný tuk? Důvodem je, že je bohatý na glycerol triestery (triglyceridy), a dřevo popel je zdrojem draslíku, základního kovu.
V opačném případě postupuje reakce na nižší výtěžek, ale dostatečně na to, aby odrážela jeho účinky na barvy a některé povrchy. Takový je případ olejomaleb, kde jsou pigmenty smíchány s olejem (zdroj esterů).
Index
- 1 Saponifikační reakce
- 1.1 Mechanismus
- 1.2 Kinetika
- 2 Látky, které lze získat zmýdelněním
- 2.1 Rozpouštědlové působení mýdel
- 3 Odkazy
Saponifikační reakce
Mechanismus
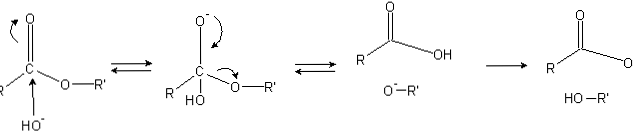
Estery mají acylovou skupinu (O = C-R), která je náchylná k nukleofilním atakům, jako je OH-.
Protože atomy kyslíku "ukradnou" elektronickou hustotu z atomu uhlíku, je částečně nabitý, dokonce ještě více v případě esterů.
V důsledku toho tento pozitivní náboj přitahuje negativní druhy schopné dodávat elektrony na atom uhlíku, přičemž dochází k nukleofilnímu útoku (levá strana obrazu). Výsledkem je vytvoření tetraedrického meziproduktu (druhá molekula zleva doprava).
Negativní náboj na kyslíku tetraedrického meziproduktu je produktem OH- okolí Pak je tento záporný náboj delokalizován tak, aby vytvořil karbonylovou skupinu, "vynucení", pak rozbití vazby C-OR '. Také toto přemístění produkuje karboxylovou kyselinu RCOOH a alkoxidový ion R'O-.
Konečně, jak je reakční prostředí bazické, alkoxid deprotonuje jednu molekulu vody a karboxylová kyselina reaguje s jiným OH- produkci produktů zmýdelnění.
Kinetika
Rychlost saponifikační reakce je úměrná koncentracím reaktantů. Jinými slovy, zvýšení koncentrace esteru (RCOOR ') nebo báze (NaOH) bude probíhat vyšší rychlostí.
To je také přeloženo následovně: míra zmýdelnění je první řád vzhledem k esteru a první pořadí vzhledem k bázi. Výše uvedené lze vyjádřit pomocí následující matematické rovnice:
Rychlost = k [RCOOR '] [NaOH]
Kde k je konstantní nebo rychlostní koeficient, který se mění jako funkce teploty nebo tlaku; to znamená, že čím vyšší je teplo, tím větší je rychlost zmýdelnění. Z tohoto důvodu je médium vystaveno varu.
Vzhledem k tomu, že obě činidla mají kinetiku prvního řádu, je celková reakce druhá.
V reakčním mechanismu zmýdelnění vyžaduje vytvoření tetraedrického meziproduktu nukleofilní atak, který zahrnuje jak ester, tak bazu..
Kinetika druhého řádu se tedy v této skutečnosti odráží, protože zasahují do (pomalého) determinantního kroku reakce.
Látky, které lze získat zmýdelněním

Hlavními produkty zmýdelnění jsou alkoholy a soli karboxylových kyselin. V kyselém prostředí se získá příslušná RCOOH, získaná zmýdelněním tuků a olejů, které jsou známé jako mastné kyseliny..
Tímto způsobem mýdla sestávají ze solí mastných kyselin vyplývajících ze zmýdelnění. Chodíte s kationty? Mohou to být Na+, K+, Mg2+, Víra3+, atd..
Tyto soli jsou rozpustné ve vodě, ale precipitují působením NaCl přidaného ke směsi, která dehydratuje mýdlo a odděluje ji od vodné fáze. Saponifikační reakce pro triglycerid je následující:
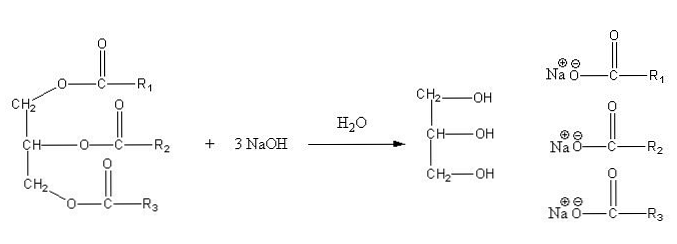
Glycerin je alkoholický "E" a mýdlem jsou všechny soli výsledných mastných kyselin. Zde má každá postranní větev -R různé délky a stupeň nenasycení. V důsledku toho tyto řetězce dělají rozdíl mezi tuky a rostlinnými oleji.
Klíč k výrobě mýdel pak spočívá ve výběru nejlepších tuků a olejů, nebo konkrétněji při výběru různých zdrojů triglyceridů..
Tato bílá mýdlová hmota může ve své struktuře obsahovat barviva a další organické sloučeniny, což jí dodává příjemné aroma a jasné barvy. Odtud je rozsah možností skroten uměním a povoláním v tomto obchodě.
Saponifikační reakce je však také syntetickou cestou karboxylových kyselin a alkoholů, které nemusí nutně souviset s glycerinem nebo mýdly..
Například základní hydrolýza jakéhokoliv esteru, jako je jednoduchý ethylacetát, poskytne kyselinu octovou a ethanol.
Rozpouštědlové působení mýdel

Soli mastných kyselin jsou rozpustné ve vodě, ale ne stejným způsobem jako ionty jsou solvatované; obklopené vodnou koulí. V případě mýdel, jejich postranní řetězy -R jim brání teoreticky v rozpouštění ve vodě.
Proto, aby se zabránilo této energeticky nepohodlné pozici, jsou orientovány takovým způsobem, že tyto řetězce přicházejí do styku, tvořící nepolární organické jádro, zatímco polární hlavy, konec (-COO)- Na+), interakci s molekulami vody a vytvoření „polárního prostředí“.
Výše uvedené je znázorněno na obrázku výše, kde je znázorněn tento typ struktury známý jako micelle.
"Černé ocasy" odpovídají hydrofobním řetězcům, které jsou zapleteny do organického jádra chráněného šedými kuličkami. Tyto šedé koule tvoří polární štít, hlavy -OO- Na+.
Pak jsou micely shluky (shluky) solí mastných kyselin. V nich mohou uzavírat tuk, který je nerozpustný ve vodě, protože má nepolární charakter.
Jak to dělají? Jak řetězec tuku, tak -R řetězce jsou hydrofobní, takže obě mají navzájem velkou afinitu.
Když micely uzavírají tuky, voda interaguje s polárním obalem, což umožňuje rozpustnost mýdla. Podobně jsou micely záporně nabité, což způsobuje vzájemné odpuzování a tím generování disperze tuku.
Odkazy
- Anne Marie Helmenstine, Ph.D. (3. října 2017). Definice a reakce zmýdelnění. Získáno 24. dubna 2018, z: thoughtco.com
- Francis A. Carey. Organická chemie Karboxylové kyseliny. (šesté vydání, str. 863-866). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. Organická chemie. Lipids (10. vydání, strana 1056-1058). Wiley Plus.
- Wikipedia. (2018). Zmydelnění. Získáno 24. dubna 2018, z: en.wikipedia.org
- Boyd C. (27. února 2015). Pochopte chemii a historii mýdla. Získáno 24. dubna 2018, z: chemservice.com
- Luca Laghi (27. března 2007). Zmydelnění. Získáno 24. dubna 2018, z: commons.wikimedia.org
- Amanda háčkování (12. května 2015). Micelle (stupně šedi). Získáno 24. dubna 2018, z: commons.wikimedia.org


