Vlastnosti dichromátu sodného, výroba, nebezpečí a použití
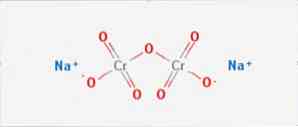
dichroman sodný "Anorganická sloučenina vzorce Na2Cr207" je anorganická sloučenina vzorce Na2Cr207. Je to jedna z mnoha sloučenin šestimocného chromu (Cr VI). Jeho struktura je znázorněna na obr. 1, i když se obvykle sůl zpracovává ve své dihydratované formě, jejíž vzorec by byl Na2Cr207..
Má dvě iontové vazby mezi molekulami sodíku a záporně nabitými kyslíky. Chrómová ruda se extrahuje z dichromanu sodného. Ročně se vyrábějí miliony kilogramů dichromanu sodného.
Čína je největším výrobcem dichromanu sodného, nicméně čínské chemické závody mají relativně nízkou produkci, méně než 50 000 tun ročně, ve srovnání s továrnou v Kazachstánu, která produkuje více než 100 000 tun ročně..
Rostliny v Rusku, ve Spojených státech a ve Spojeném království mají meziroční produkci mezi 50 000 a 100 000 tun ročně (Kogel, 2006).
Co se týče reaktivity a vzhledu, dichroman sodný má vlastnosti podobné dichromanu draselnému, avšak sodná sůl je rozpustnější ve vodě a má hmotnostní ekvivalent menší než draselná sůl..
Dichroman sodný vytváří při zahřívání toxické výpary chrómu. Je to silné oxidační činidlo a je vysoce korozivní.
Tato sloučenina se nachází v zdrojích pitné vody kontaminovaných různými průmyslovými postupy, jako jsou techniky galvanizace nebo galvanizace, opalování kůže a textilní výroba..
Index
- 1 Fyzikální a chemické vlastnosti
- 2 Výrobní metody
- 3 Reaktivita a nebezpečí
- 4 Použití a aplikace
- 5 Biochemie
- 6 Odkazy
Fyzikální a chemické vlastnosti
Dvojchroman sodný se skládá z krystalů s červeno-oranžovou monoklinickou strukturou ve formě bezvodé a bez zápachu. Jeho molekulová hmotnost je 261,97 g / mol ve své bezvodé formě a 298,00 g / mol ve své dihydratované formě..
Má bod tání 356,7 ° C, bod varu 400 stupňů Celsia, ve kterém se rozkládá. Má hustotu 2,52 g / ml.

Obrázek 2 ukazuje vzhled dichromanu sodného. Jeho rozpustnost ve vodě je 187 g na 100 gramů při 25 stupních Celsia a její rozpustnost v ethanolu je 513,2 gramů na litr při teplotě 19,4 ° C (National Center for Biotechnology Information, s.f.)..
Považuje se za stabilní látku, pokud je skladován za doporučených podmínek a není hořlavý. Vzhledem k tomu, že se jedná o silné oxidační činidlo, je korozivní a v roztoku je kyselina, která má schopnost snížit pH na 4 v roztoku 1% hmotn./obj..
Výrobní metody
Chroman sodný může být převeden na dichroman kontinuálním procesem, který zpracovává kyselinou sírovou, oxidem uhličitým nebo kombinací těchto dvou látek..
Odpařování roztoku dichromanu sodného způsobí vysrážení síranu sodného a / nebo hydrogenuhličitanu sodného a tyto sloučeniny se odstraní před konečnou krystalizací dichromanu sodného..
Dvojchroman sodný může být proveden v třístupňovém procesu:
- Alkalické pražení chromitových oxidačních podmínek
- Vyluhování. Extrakce rozpustné látky ze směsi působením kapalného rozpouštědla
- Konverze monochromátu sodného v dichromanu sodném pomocí kyseliny.
Bezvodý dichroman sodný se může připravit roztavením dihydrátu dihydrátu sodného, krystalizací vodných roztoků dichromanu nad 86 ° C nebo sušením roztoků dichromanu sodného ve sprejových sušičkách..
Roztoky dvojchromanu sodného o koncentraci 69 a 70% w / v se používají jako pohodlný a nákladově efektivní způsob odesílání množství, čímž se zabrání nutnosti manuální manipulace nebo rozpouštění krystalů..
Reaktivita a nebezpečí
Je to silné oxidační činidlo. Neslučitelný se silnými kyselinami. Kontakt s hořlavými materiály může způsobit požár. V přítomnosti tepla nebo ohně mohou vznikat toxické páry oxidu chromitého.
Známá "směs kyseliny chromové" dichromanu a kyseliny sírové s organickými zbytky vede k prudké exotermní reakci. Tato směs v kombinaci s acetonovými zbytky také vede k prudké reakci.
Kombinace dichromanu a kyseliny sírové s alkoholy, ethanolem a 2-propanolem vede k prudké exotermní reakci. Vzhledem k výskytu mnoha incidentů zahrnujících míchání kyseliny dichromové a kyseliny sírové s oxidovatelnými organickými materiály je pravděpodobně nejlepší se těmto interakcím vyhnout..
Kombinace dichromanu s hydrazinem je výbušná, lze očekávat, že dichromátová reakce bude silná s aminy obecně. Přidání dehydratované dichromátové soli do anhydridu kyseliny octové vede ke konečné explozivní exotermní reakci.
Bor, křemík a dichromany tvoří pyrotechnické směsi. Směs kyseliny octové, 2-methyl-2-pentenal a dichromanu vede k nekontrolovatelné reakci (Chemical Datasheet Sodium Dichromate., 2016).
Vdechnutí prachu nebo mlhy způsobuje podráždění dýchacích cest, které se někdy podobá astmatu. Může dojít k septální perforaci. Je považován za jed.
Požití způsobuje zvracení, průjem a velmi neobvykle komplikace žaludku a ledvin. Kontakt s očima nebo kůží způsobuje místní podráždění. Opakovaná expozice pokožce způsobuje dermatitidu.
Dvojchroman sodný je karcinogen u lidí. Existují důkazy, že šestimocné sloučeniny chrómu nebo Cr (VI) mohou u lidí způsobit rakovinu plic. Bylo prokázáno, že dichroman sodný způsobuje rakovinu plic u zvířat.
Ačkoli dvojchroman sodný nebyl identifikován jako teratogenní sloučenina nebo reprodukční riziko, je známo, že šestimocné sloučeniny chrómu nebo Cr (VI) jsou teratogenní a způsobují reprodukční poškození, jako je snížení plodnosti a narušování menstruačních cyklů..
Dvojchroman sodný může způsobit poškození jater a ledvin, proto musí být zvládnut s extrémní péčí (New Jersey Department of Health, 2009).
V případě požití by oběť měla pít vodu nebo mléko; nikdy nevyvolávejte zvracení. V případě kontaktu s kůží nebo očima je třeba postupovat jako s kyselými popáleninami; Oči vypláchněte vodou nejméně 15 minut.
Vnější léze mohou být otírány 2% roztokem thiosíranu sodného. Ve všech případech by měl být konzultován lékař.
Použití a aplikace
Kromě jeho důležitosti při výrobě jiných chrómových chemikálií má dichroman sodný také mnoho přímých použití jako přísada při výrobě:
- Kovová povrchová úprava: napomáhá korozní odolnosti a čistí kovové povrchy, také podporuje přilnavost barvy.
- Organické produkty: používají se jako oxidační činidla při výrobě produktů, jako je vitamin K a vosk.
- Pigmenty: používají se při výrobě anorganických chromátových pigmentů, kde produkují řadu barev stabilních vůči světlu. Některé druhy chromátu jsou také používány jako inhibitory koroze ve spodních vrstvách a primerech.
- Keramika: používá se při přípravě barevných skel a keramických glazur.
- Textil: používá se jako mořidlo pro kyselá barviva pro zlepšení jeho rychle zbarvených vlastností.
- Výroba síranu chromitého.
(Dvojchroman sodný, stavební blok pro prakticky všechny ostatní sloučeniny chrómu, 2010-2012)
Dihydrát dvojchromanu sodného, jeho použití je ideální v různých podmínkách, včetně aplikací s vysokou teplotou, jako jsou keramické glazury a barevné sklo..
Oxid chromitý, který je tvrdší než jiné oxidy kovů, jako je titan nebo železo, je ideální pro prostředí, kde jsou teploty a provozní podmínky agresivní..
Tato látka se používá hlavně k výrobě jiných sloučenin chrómu, ale používá se také v bentonitových kalech používaných při výrobě ropy, v prostředcích na ochranu dřeva, při výrobě organických chemikálií a jako inhibitor koroze..
Když se smísí s hliníkem a dichromanem draselným, za použití alumino-termického procesu, oxid chromitý produkuje vysoce čistý kovový chrom. To je zásadní složka při výrobě vysoce výkonných vysoce legovaných slitin používaných v leteckém a kosmickém průmyslu.
V organické syntéze se dichroman sodný používá jako oxidační činidlo při redukčních oxidových reakcích v přítomnosti kyseliny sírové.
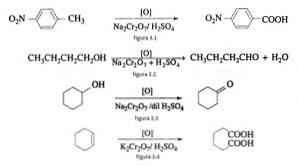
Například oxidace p-nitrotoluenu za vzniku kyseliny p-nitrobenzoové, při oxidaci n-butanolu za vzniku n-butaldehydu, při tvorbě cyklohexanonu z cyklohexanolu a při tvorbě kyseliny adipové podle obrázků 3.1. 3.2, 3.3 a 3.4 (VK Ahluwalia, 2004).
Biochemie
Intratracheální instilace dichromanu sodného (CrVI) a hydroxidu octanu chromitého (CrIII) u samců krys vedla ke zvýšení koncentrací chrómu v plné krvi, plazmě a moči až do 72 hodin po expozici; Maximální koncentrace byly dosaženy za 6 hodin po expozici.
Poměr mezi koncentrací chrómu v plné krvi a plazmatického chromu byl pro ošetření Cr (VI) a Cr (III) výrazně odlišný. Pro vyhodnocení expozice chromu by proto měly být použity analýzy chromu v krvi a chromu v plazmě.
Chrom byl také detekován v periferních lymfocytech. Cr (VI), ale ne Cr (III) se po léčbě akumuloval významně v lymfocytech. Tyto buňky mají potenciál být použity jako biomarkery při hodnocení expozice sloučeninám chrómu (Hooth, 2008).
Odkazy
- Chemický datový list Dichromát sodný. (2016). Získané z chemikálií cameo: cameochemicals.noaa.
- Hooth, M. J. (2008). Technická zpráva o toxikologii a studiích karcinogeneze dihydrátu dichromanu sodného. Národní institut zdraví USA.
- Kogel, J. E. (2006). Průmyslové nerosty a skály: Komodity, trhy, a používá sedmé vydání. littleton colorado: společnost těžby, metallurgyc a průzkum vč.
- Národní centrum pro biotechnologické informace. (s.f.). PubChem Compound Database; CID = 25408. Zdroj: pubchem.com: pubchem.ncbi.nlm.nih.gov.
- New Jersey ministerstvo zdraví. (2009, listopad). informační list o nebezpečných látkách dvojchroman sodný. Zdroj: nj.gov: nj.gov.
- Dvojchroman sodný. Stavební blok pro prakticky všechny ostatní sloučeniny chrómu. (2010–2012). Zdroj: elementis chromium: elementischromium.com
- K. Ahluwalia, R. A. (2004). Komplexní praktická organická chemie: Příprava a kvantitativní analýza. Delhi: Univerzitní tisk (Indie).


