Cesty pentózových fází a příbuzných nemocí
cesta pentóz Fosfát, také známý jako odchylka monofosfátu hexóz, je základní metabolickou dráhou, která má jako konečný produkt ribozomy, nezbytné pro cesty syntézy nukleotidů a nukleových kyselin, jako je DNA, RNA, ATP, NADH, FAD a koenzym A.
Produkuje také NADPH (nikotinamidadenindinukleotid fosfát), který se používá v různých enzymatických reakcích. Tato cesta je velmi dynamická a schopná přizpůsobit své produkty v závislosti na momentálních potřebách buněk.
ATP (adenosintrifosfát) je považován za "energetickou měnu" buňky, protože její hydrolýza může být spojena s celou řadou biochemických reakcí..
Stejně tak je NADPH druhou nezbytnou energetickou měnou pro redukční syntézu mastných kyselin, syntézu cholesterolu, syntézu neurotransmiterů, fotosyntézu a detoxikační reakce..
Ačkoli NADPH a NADH mají podobnou strukturu, nemohou být v biochemických reakcích zaměnitelné. NADPH se podílí na využití volné energie při oxidaci určitých metabolitů pro redukční biosyntézu.
Oproti tomu se NADH podílí na využití volné energie z oxidace metabolitů pro syntézu ATP.
Index
- 1 Historie a umístění
- 2 Funkce
- 3 Fáze
- 3.1 Oxidační fáze
- 3.2 Neoxidační fáze
- 4 Související nemoci
- 5 Odkazy
Historie a umístění
Údaje o existenci této trasy začaly v roce 1930 díky vyšetřovateli Ottovi Warburgovi, kterému byl nález NADP přičítán.+.
Některá pozorování umožnila objevení cesty, zejména pokračování respirace v přítomnosti inhibitorů glykolýzy, jako je fluoridový iont..
Potom v roce 1950 vědci Frank Dickens, Bernard Horecker, Fritz Lipmann a Efraim Racker popsali pentózovou fosfátovou dráhu.
Tkáně, které se podílejí na syntéze cholesterolu a mastných kyselin, jako jsou mléčné žlázy, tuková tkáň a ledviny, mají vysoké koncentrace enzymů fosfátu pentózy..
Játra jsou také důležitou tkání pro tuto dráhu: přibližně 30% oxidace glukózy v této tkáni nastává díky enzymům pentózové fosfátové cesty..
Funkce
Pentose fosfátová cesta je zodpovědná za udržování homeostázy uhlíku v buňce. Podobně tato cesta syntetizuje prekurzory nukleotidů a molekul zapojených do syntézy aminokyselin (strukturní bloky peptidů a proteinů)..
Je hlavním zdrojem redukční energie pro enzymatické reakce. Kromě toho poskytuje nezbytné molekuly pro anabolické reakce a pro obranné procesy proti oxidačnímu stresu. Poslední fáze dráhy je kritická v redox procesech ve stresových situacích.
Fáze
Pentase fosfátová cesta se skládá ze dvou fází v buněčném cytosolu: oxidačním, který generuje NADPH s oxidací glukóza-6-fosfátu na ribóza-5-fosfát; a neoxidační, což zahrnuje vzájemnou přeměnu cukrů tří, čtyř, pěti, šesti a sedmi uhlíků..
Tato cesta představuje společné reakce s Calvinovým cyklem as Entner-Doudoroffovou cestou, která je alternativou glykolýzy.
Oxidační fáze
Oxidační fáze začíná dehydrogenací molekuly glukózy-6-fosfátu na uhlíku 1. Tato reakce je katalyzována enzymem glukóza-6-fosfátdehydrogenáza, která má vysokou specificitu NADP+.
Produktem této reakce je 6-fosfonoglukono-8-lakton. Potom se tento produkt hydrolyzuje enzymem laktonasou za vzniku 6-fosfoglukonátu. Tato sloučenina je přijata enzymem 6-fosfoglukonátdehydrogenázou a stává se ribulózo-5-fosfátem.
Enzym fosfopentose izomeráza katalyzuje konečný krok oxidační fáze, který zahrnuje syntézu ribózy 5-fosfátu izomerací ribulóza 5-fosfátu..
Tato série reakcí produkuje dvě molekuly NADPH a jednu molekulu ribózy 5-fosfátu na molekulu glukózového 6-fosfátu, která vstupuje do této enzymatické dráhy.
V některých buňkách jsou požadavky na NADPH větší než požadavky na ribóza 5-fosfát. Enzymy transketolasy a transaldolasy proto užívají ribóza 5-fosfát a přeměňují ji na glyceraldehyd-3-fosfát a fruktózo-6-fosfát, což vede k neoxidační fázi. Tyto poslední dvě sloučeniny mohou vstoupit do glykolytické dráhy.

Neoxidační fáze
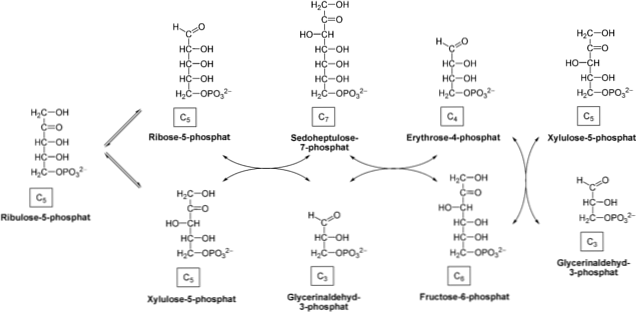
Fáze začíná epimerizační reakcí katalyzovanou enzymem pentose-5-fosfát epimeráza. Ribulose-5-fosfát se odebírá tímto enzymem a převádí na xylulóza-5-fosfát.
Produkt je absorbován enzymem transketolasy, který působí společně s koenzymem thiamin-pyrofosfátem (TTP), který katalyzuje průchod xylulóza-5-fosfátu na ribóza-5-fosfát. Při přenosu ketózy na aldózu se produkují glyceraldehyd-3-fosfát a sedoheptulosa-7-fosfát..
Enzym transaldolasy dále přenáší C3 ze molekuly sedoheptulosa-7-fosfátu na glyceraldehyd-3-fosfát, který produkuje cukr se čtyřmi uhlíky (erythrosa-4-fosfát) a cukr se šesti uhlíky (fruktóza-6). -fosfát). Tyto produkty jsou schopné živit glykolytickou dráhu.
Enzym transketosala působí znovu, aby přenesl C2 xylulóza-5-fosfátu na erythrose-4-fosfát, což vede k fruktosa-6-fosfátu a glyceraldehyd-3-fosfátu. Stejně jako v předchozím kroku mohou tyto produkty vstoupit do glykolýzy.
Tato druhá fáze spojuje cesty, které generují NADPH s těmi, které jsou zodpovědné za syntézu ATP a NADH. Kromě toho, produkty fruktosa-6-fosfát a glyceraldehyd-3-fosfát mohou vstoupit do glukoneogeneze.
Související nemoci
Různé patologie souvisejí s cestou fosfátu pentózy, mezi těmito neuromuskulárními onemocněními a různými typy rakoviny.
Většina klinických studií se zaměřuje na kvantifikaci aktivity glukóza-6-fosfátdehydrogenázy, protože je hlavním enzymem zodpovědným za regulaci dráhy..
V krevních buňkách patřících jedincům náchylným k anémii mají nízkou enzymatickou aktivitu glukóza-6-fosfátdehydrogenázy. Naopak buněčné linie související s karcinomy v hrtanu vykazují vysokou enzymatickou aktivitu.
NADPH se podílí na produkci glutathionu, klíčové peptidové molekuly v ochraně proti reaktivním kyslíkovým druhům, zapojeným do oxidačního stresu.
Různé typy rakoviny vedou k aktivaci pentózové dráhy a jsou spojeny s metastázami, angiogenezí a reakcemi na chemoterapii a radioterapii..
Na druhé straně, chronická granulomatózní choroba se vyvíjí, když je nedostatek produkce NADPH.
Odkazy
- Berg, J. M., Tymoczko, J. L., Stryer, L (2002). Biochemie. WH Freeman
- Konagaya, M., Konagaya, Y., Horikawa, H., & Iida, M. (1990). Pentose-fosfátová cesta při neuromuskulárních onemocněních - hodnocení aktivity svalové glukózy 6-fosfátdehydrogenázy a obsahu RNA. Rinsho shinkeigak. Klinická neurologie, 30(10), 1078-1083.
- Kowalik, M.A., Columbano, A., & Perra, A. (2017). Rozvíjející se úloha pentózo-fosfátové dráhy u hepatocelulárního karcinomu. Hranice v onkologii, 7, 87.
- Patra, K. C., & Hay, N. (2014). Pentose fosfátová cesta a rakovina. Trendy v biochemických vědách, 39(8), 347-354.
- Stincone, A., Prigione, A., Cramer, T., Wamelink, M., Campbell, K., Cheung, E., ... & Keller, M. A. (2015). Návrat metabolismu: biochemie a fyziologie cesty fosforečnanu pentózy. Biologické recenze, 90(3), 927-963.
- Voet, D., & Voet, J. G. (2013). Biochemie. Umělecký vydavatel.


